含锌废渣和各种锌矿(如菱锌矿)都有着重要的用途
I.以含锌废渣(主要成分为
,杂质为
﹑
)为原料制备七水硫酸锌(
)的流程如下。

(1)粉碎的目的是
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要的玻璃仪器有胶头滴管﹑玻璃棒﹑
(3)物质X是
(4)流程中获得七水硫酸锌前省略的操作是
(5)某温度下,
分解得到一种铁﹑氧质量比21:8的氧化物,该氧化物的化学式
(6)除铁过程中,温度pH对除铁效果的影响分别对如图所示。由图可知,除铁时温度应控制在

II.以某菱锌矿(
含量为62.5%)为原料制备锌的原理如下(假设杂质不参加反应):
则100吨这样的菱锌矿理论上最多制得锌多少吨?(写出计算过程)
图1 是实验室里测定氧气含量的装置。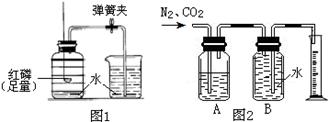
(1)红磷在空气中燃烧的现象,写出该反应的化学方程式。
(2)当红磷熄灭并冷却到室温后,打开弹簧夹,看到的现象是。
(3)待红磷熄灭并完全冷却到室温打开弹簧夹,结果实验测定结果仍偏低。可能的原因是。
(4)上述实验提供了一种粗略测定混合气体中某种气体体积含量的方法。如果要测定氮气、二氧化碳混合气体中二氧化碳的体积含量,可将一定体积的混合气体样品通入图2所示的装置。其中A瓶中装有足量的溶液,实验结束后,量筒中的水的体积约等于的体积。
下图是实验室制取气体常用的装置。
⑴若用A装置制取氧气,反应的化学方程式为________________________________;
⑵若用B装置制取氧气,反应的化学方程式为________________________________;B装置中棉花的作用;可用C装置收集氧气的依据____;收集满氧气后,先将导管移出水面,再熄灭酒精灯的目的是___________________________;
⑶若用D装置收集氧气,导管口要接近集气瓶底部的原因______________________,验证氧气已经收集满的方法是_______________________________________________。
写出下列反应的化学方程式,并注明反应的基本类型。
(1)燃烧木炭取暖、
(2)实验室加热氯酸钾制氧气、
我们每时每刻都离不开氧气,通过学习我们知道氧气约占空气体积的;缓慢氧化是物质与氧气发生的一种不易察觉的反应,有时人们可以利用缓慢氧化,但有时缓慢氧化也会给人们带来麻烦和损失。请从日常生活中各举一个实例。有利的实例:;不利的实例:;空气一旦被污染,危害非常大,写出一种能造成空气污染的情况。
近两年来,我国西南、北方、长江中下游等地先后遭遇大范围持续干旱。水是生命之源,我们应该了解水、爱护水资源。
(1)有些村庄打深井取用地下水,可用区分地下水是软水还是硬水,硬水会给生活和生产带来许多麻烦,请举一例说明使用硬水的危害,生活中常采用的方法降低水硬度。
(2)人们利用吸附、沉淀、过滤和蒸馏等方法净化水,其中净化程度最高的操作是。
(3)水体污染的来源主要有工业污染、农业污染、______________。
(4)小明同学为了探究水的组成,做了水的电解实验,发现两极上都有气泡冒出,其中正极与负极上的气体体积之比约为1:2,经检验,正极上产生的气体是,写出电解水的化学方程式。
(5)“节约用水,从我做起。”请你任举一例生活中节约用水的措施:。