(14)铬是一种银白色金属,化学性质稳定,以+2、+3和+6价为常见价态。工业上以铬铁矿(主要成分为FeO·Cr2O3 ,含有Al2O3、SiO2等杂质)为主要原料生产金属铬和重铬酸钠Na2Cr2O7·2H2O(已知Na2Cr2O7是一种强氧化剂),其主要工艺流程如下:
查阅资料得知:
①常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-
②常温下,Ksp[Cr(OH)3]=6.3×10-31
回答下列问题:
(1)工业上常采用热还原法制备金属铬,写出以Cr2O3为原料,利用铝 热反应制取金属铬的化学方程式 。
(2)酸化滤液D时,不选用盐酸的原因是 。
(3)固体E的主要成分是Na2SO4,根据下图分析操作a为 、 。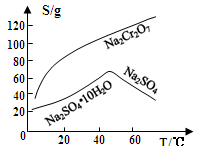
(4)已知含+6价铬的污水会污染环境。电镀厂产生的镀铜废水中往往含有一定量的Cr2O72-,处理该废水常用还原沉淀法,具体流程如下:
①Cr(OH)3的化学性质与Al(OH)3相似。在上述生产过程中加入NaOH溶液时要控制溶液的pH不能过高,是因为 ;
②下列溶液中可以代替上述流程中Na2S2O3溶液的是 (填选项序号);
| A.FeSO4溶液 | B.浓H2SO4 | C.酸性KMnO4溶液 | D.Na2SO3溶液 |
③调整溶液的pH=5时,通过列式计算说明溶液中的Cr3+是否沉淀完全 ;
④上述流程中,每消耗0.1molNa2S2O3转移0.8mole-,则加入Na2S2O3溶液时发生反应的离子方程式为 。
请按要求分别设计一个简单易行的验证实验。
(1)验证钠和镁的金属性强弱;
(2)验证硫和氯的非金属性强弱。
现在V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20,其中V的一种原子的原子核内没有中子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍,Y元素原子最外层电子数是X元素原子最外层电子数的两倍;X、Z是金属元素,Z的核外电子排布与Ar原子相同。请回答:
(1)V是,X是,Z是(填元素符号)
(2)Y在周期表中的位置是;
(3)V和W形成V2W型化合物的电子式为,所含的化学键类型为;
(4)用电子式表示Z和Y形成化合物的过程是。
现有A、B、C、D四种元素,A元素形成的—2价阴离子比氦原子的核外电子数多8个,B元素与A元素形成的一种化合物为淡黄色固体,该固体遇到空气能生成A的单质;C为原子核内有12个中子的金属元素,当2.4克C与足量热水反应时,在标准状况下放出气体2.24L,C形成正二价阳离子;D元素原子的M层上有7个电子。
(1)写出B、C两种元素的元素符号:B,C;
(2)画出A2-的离子结构示意图:,
指出D在周期表的位置: ;
;
(3)写出B的呈淡黄色的化合物与CO2反应的化学方程式:;
(4)比较D的气态氢化物与H2S和HF的稳定性:(用化学式表示);
(5)用电子式表示C与D形成化合物的过程:。
已知A是灰黑色的硬而脆的固体,B是气态物质,A~E各种物质的相互转化关系如下图所示。
(1)写出B、D、E三种物质的化学式: B ,D ,E ;
B ,D ,E ;
(2)画出A的原子结构示意图 ;
(3)写出C→A的化学方程式 。
除去下列溶液的少量杂质,根据要求填空。
| 物质 |
杂质 |
选用试剂 |
离子方程式 |
| NaNO3 |
NaCl |
||
| KCl |
K2CO3 |
||
| NaHCO3 |
Na2CO3 |