设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.1 mol FeI2与足量氯气反应时转移的电子数为2NA |
| B.1 L 1mol/L的盐酸含有NA个HCl分子 |
| C.标准状况下,33.6 L四氯化碳中含有氯原子的数目为6NA |
D.5NH4NO3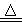 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA |
用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是
①加盐酸溶解②加烧碱溶液溶解③过滤④通入过量CO2生成Al(OH)3沉淀
⑤加入盐酸生成Al(OH)3 沉淀⑥加入过量烧碱溶液
| A.①⑥⑤③ | B.②③④③ | C.②③⑤③ | D.①③⑤③ |
在一密闭气缸内,用不漏气的可滑动的活塞隔成两室,左边充有氮气,右边充有氢气和氧气的混合气体,如下图所示。在室温下,将右边的混合气体点燃,反应后冷却到室温,活塞最终静止在气缸的中点。则原混合气体中氢气与氧气的体积比可能是
| A.2: 7 | B.7:2 | C.5: 4 | D.8:1 |
下列叙述正确的是
| A.向含有 CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成 |
| B.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2 |
| C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同 |
| D.向Na2CO3饱和溶液中通入CO2有NaHCO3结晶析出 |
在下列给定的溶液中一定能大量共存的离子组是
| A.Kw/c(H+)=0.lmol/L的溶液中:K+、Fe2+、Cl—、NO3— |
| B.水电离的H+浓度为1×10-12 mol/L的溶液:K+、Ba2+、Cl—、Br— |
| C.加入NH4HCO3固体产生气泡的溶液中:Na+、Mg2+、ClO—、S2- |
| D.加金属铝能产生氢气的溶液中:Ca2+、NH+4、Cl—、HSO—3 |
设NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.常温常压下4.6g NO2和N2O4混合气体所含原子总数为0.3NA |
| B.标准状况下,22.4L SO3的分子数为NA |
| C.将标准状况下11.2L的Cl2通入足量水中发生反应,转移的电子总数为0.5NA |
| D.电解58.5 g熔融的NaCl,能产生22.4 L氯气(标准状况)、23.0 g金属钠 |