将2.3g Na和2.7g Al同时加入到足量的水中充分反应,将反应后的溶液稀释、定容为500mL.下列说法正确的是
| A.整个反应过程中共转移电子0.4 mol |
| B.反应产生的气体在标准状况下的体积是1.12L |
| C.反应所得溶液与足量CO2反应的离子方程式:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D.在稀释、定容操作中用到的全部玻璃仪有:烧杯、玻璃棒、500mL容量瓶 |
混合下列各组物质使之充分反应,加热蒸干产物并高温下灼烧至质量不变,最终残留固体为纯净物的是
| A.向CuSO4溶液中加入适量铁粉 |
| B.在Na2SiO3溶液中通入过量CO2气体 |
| C.等物质的量的NaHCO3与Na2O2溶于水 |
| D.等物质的量浓度、等体积的FeCl3与KI溶液混合 |
下列离子方程式正确的是
| A.将少量Na2O2粉末加入到H218O水中:2H218O+2Na2O2═4Na++4OH﹣+18O2↑ |
| B.向AlC13溶液中加入过量的氨水: Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| C.氯化亚铁溶液中通入足量C12: Fe2++C12 =Fe3++2C1- |
| D.往NH4HSO4溶液中加入足量NaOH溶液: NH4++H++2OH-=NH3·H2O+H2O |
下列冶炼金属的原理正确的是
A.2A12O3+3C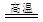 A1+3CO2↑ A1+3CO2↑ |
B.MgO十H2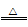 Mg+H2O Mg+H2O |
C.Fe3O4+4CO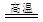 3Fe+4CO2 3Fe+4CO2 |
D.2HgO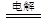 2Hg+O2↑ 2Hg+O2↑ |
对于下列常见化学的认识错误的是
| A.明矾可用作净水剂 |
| B.干冰能用于人工降雨 |
| C.小苏打是一种膨松剂,可用于制作馒头和面包 |
| D.碳酸钙是文物陶瓷的主要成分 |