(12分)氢溴酸在医药和石化工业上有广泛用途.图1是模拟工业制备氢溴酸的流程:
回答下列问题:
(1)混合①中发生反应的离子方程式为 .
(2)混合②中加入试剂a是 .
(3)加入Na2SO3的目的是除去过量的Br2,但要防止过量,原因是 (请用离子方程式表示).
(4)工业氢溴酸常带有淡淡的黄色,可能的原因是:①含Fe3+②含Br2③含Fe3+和Br2,只用下列一种试剂就能分析产生淡黄色的原因.该试剂是 (填写字母).
a.KMnO4溶液
b.NaOH溶液
c.KSCN溶液
d.淀粉KI溶液
e.CCl4
(5)实验室制取Br2的反应为:2NaBr+3H2SO4+MnO2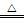 2NaHSO4+MnSO4+Br2↑+2H2O制取Br2最好选用图2装置中的 (填写字母,固定和加热装置均已省略).简述检验已选定的图2装置气密性的方法 .
2NaHSO4+MnSO4+Br2↑+2H2O制取Br2最好选用图2装置中的 (填写字母,固定和加热装置均已省略).简述检验已选定的图2装置气密性的方法 .
有硫酸酸化的草酸(H2C2O4,二元弱酸)溶液能将KMnO4溶液中的MnO4-转化为Mn2+。某化学小组研究发现,少量MnSO4可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,完成以下实验设计表。
| 实验 编号 |
温度 |
初始pH |
0.1 mol/L草酸溶液/mL |
0.01mol/LKMnO4溶液体积/mL |
蒸馏水 体积/mL |
待测数据(反应混合液褪色时间/s) |
| ① |
常温 |
1 |
20 |
50 |
30 |
t1 |
| ② |
常温 |
2 |
20 |
50 |
30 |
t2 |
| ③ |
常温 |
2 |
40 |
__________ |
______ |
t3 |
(2)该反应的离子方程式_______________________________。
(3)若t1<t2,则根据实验①和②得到的结论是_______________________________。
(4)请你设计实验验证MnSO4对该反应起催化作用,完成下表中内容。
| 实验方案(不要求写出具体操作过程) |
预期实验结果和结论 |
_________________________ |
_________________________ |
(5)化学小组滴定法测定KMnO4溶液物质的量浓度:取ag草酸晶体(H2C2O4•2H2O,摩尔质量126g/mol)溶于水配成250mL溶液,取25. 00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定两次,平均消耗KMnO4溶液VmL。滴定到达终点的现象是: _______________________;实验中所需的定量仪器有________________(填仪器名称)。该KMnO4溶液的物质的量浓度为_______mol/L。
氨基甲酸铵(NH2COONH4)是一种白色固体,受热易分解。某小组模拟制备氨基甲酸铵,反应如下(且温度对反应的影响比较灵敏):2NH3(g)+CO2(g) NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0
(1)如用下图I装置制取氨气,可选择的试剂是。
(2)制备氨基甲酸铵的装置如下图Ⅱ所示,把NH3和CO2通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中。当悬浮物较多时,停止制备。
注:CCl4与液体石蜡均为惰性介质。
① 发生器用冰水冷却的原因是,液体石蜡鼓泡瓶的作用是。
②从反应后的混合物中分离出产品的实验方法是(填写操作名称)。为了得到干燥产品,应采取的方法是(填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.减压40℃以下烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种。
①设计方案,进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
| 实验步骤 |
预期现象和结论 |
| 步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解。 |
得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置 |
若溶液不变浑浊,证明固体中不含碳酸铵。 |
| 步骤3:向试管中继续加入 。 |
,证明固体中含有碳酸氢铵。 |
②根据①的结论:取氨基甲酸铵样品3.95 g,用足量氢氧化钡溶液充分处理后,过滤、洗涤、干燥,测得沉淀质量为1.97 g。则样品中氨基甲酸铵的物质的量分数为。[Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(BaCO3)=197]
我市某地的煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下: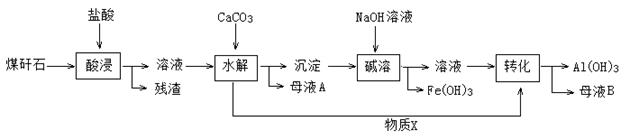
已知:
| 离子 |
开始沉淀pH |
完全沉淀pH |
| Fe3+ |
2.1 |
3.2 |
| Al3+ |
4.1 |
5.4 |
请回答下列问题:
(1)“酸浸”后得到的残渣中主要含有的物质是_________。物质X的化学式为_______。
(2)“酸浸”时影响铝浸出率的因素可能有(写出两个)____________、__________。
(3)为了获得产品Al(OH)3,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续操作过程是____________________。
(4)Al(OH)3可添加到塑料中作阻燃剂的原因是。
(5)以Al和MnO2为电极,与NaCl和稀氨水电解质溶液组成一种新型电池,放电时MnO2转化为MnO(OH)。该电池反应的化学方程式是。
(6)预处理后的100t煤矸石经上述流程后,得到39t纯度为95%的氢氧化铝产品。则预处理后的100t煤矸石中铝元素的回收率为。
某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究。
【查阅资料】SO2Cl2名称是氯化硫酰,常温下是无色液体,极易水解,遇潮湿空气会产生白雾。
【讨论】(1)SO2Cl2中S元素的化合价是。
(2)实验中制取的SO2和Cl2在混合前都必须提纯和干燥。
【实验探究】(1)实验中制得了干燥纯净的SO2和Cl2。
(2)按下图收集满Cl2后,再通入SO2,集气瓶中立即有无色液体产生,充分反应后,将无色液体和剩余气体分离,分别对无色液体和剩余气体进行如下探究。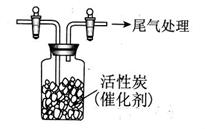
Ⅰ.探究反应产物。
向所得无色液体中加入水,立即产生白雾,振荡,静置,得无色溶液。经检验:该无色溶液中的阴离子(除OH-外)只有SO42-、Cl-。证明无色液体为SO2Cl2。
(1)SO2Cl2与水反应的化学方程式是。
(2)验证无色溶液中含有Cl-的方法是。
Ⅱ.探究反应进行的程度。
用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再加入BaCl2溶液,立即产生白色沉淀。
证明SO2与Cl2的反应是可逆反应。
阐述证明SO2与Cl2是可逆反应的理由。
【质疑】有同学提出:选修四教材习题中介绍SOCl2(亚硫酰氯)常温下是无色液体,极易水解,遇潮湿空气也会产生白雾。SO2与Cl2反应若还能生成SOCl2则无法证明生成的是SO2Cl2。
SO2Cl2与水反应的化学方程式是。
小组讨论后认为不会生成SOCl2,理由是。
(本题16分)钒是一种重要的合金元素,还用于催化剂和新型电池。从含钒固体废弃物(含有SiO2、Al2O3及其他残渣)中提取钒的一种新工艺主要流程如图:
| 物质 |
V2O5 |
NH4VO3 |
VOSO4 |
(VO2)2SO4 |
| 溶解性 |
难溶 |
难溶 |
可溶 |
易溶 |
部分含钒化合物在水中的溶解性如上表:
请回答下列问题:
(1)反应①所得溶液中除H+之外的阳离子有___________。
(2)反应②碱浸后滤出的固体主要成分是(写化学式)。
(3)反应④的离子方程式为。
(4)25℃、101 kPa时,ⅰ、4Al(s)+3O2(g) 2Al2O3(s) ΔH1=-a kJ/mol
2Al2O3(s) ΔH1=-a kJ/mol
ⅱ、4V(s)+5O2(g) 2V2O5(s)ΔH2=-b kJ/mol
2V2O5(s)ΔH2=-b kJ/mol
用V2O5发生铝热反应冶炼金属钒的热化学方程式是。
(5)钒液流电池(如图所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过。电池放电时负极的电极反应式为,电池充电时阳极的电极反应式是。
(6)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应①后溶液中的含钒量,反应的离子方程式为:2V +H2C2O4+2H+
+H2C2O4+2H+ 2VO2++2CO2↑+2H2O。取25.00 mL 0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0 mL,由此可知,该(VO2)2SO4溶液中钒的含量为g/L。
2VO2++2CO2↑+2H2O。取25.00 mL 0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0 mL,由此可知,该(VO2)2SO4溶液中钒的含量为g/L。