对于反应中的能量变化,表述正确的是
| A.吸热反应中,反应物的总能量大于生成物的总能量 |
| B.形成化学键的过程会释放能量 |
| C.加热才能发生的反应一定是吸热反应 |
| D.氧化反应均为吸热反应 |
在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是()
① K+、Cl-、NO3-、S2-② K+、Fe2+、I-、SO42-③ Na+、Cl-、NO3-、SO42-
④Na+、Ca2+、Cl-、HCO3-⑤ K+、Ba2+、Cl-、NO3-
| A.①③ | B.③⑤ | C.③④ | D.②⑤ |
用食用白醋(醋酸浓度约1 mol•L-1)进行下列实验,能证明醋酸为弱电解质的是()
| A.白醋中滴入石蕊试液呈红色 | B.白醋加入豆浆中有沉淀产生 |
| C.蛋壳浸泡在白醋中有气体放出 | D.pH试纸显示白醋的pH为2~3 |
某温度下,反应SO2(g)+ 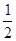 O2(g)
O2(g)  SO3 (g) 的平衡常数K1=50,在同一温度下,反应2SO3(g)
SO3 (g) 的平衡常数K1=50,在同一温度下,反应2SO3(g)  2SO2(g) + O2(g)的平衡常数K2的值为()
2SO2(g) + O2(g)的平衡常数K2的值为()
| A.2500 | B.100 | C.4×10-4C | D.2×10-2 |
某温度时,一定压强下的密闭容器中发生反应:aX(g)+bY(g) 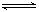 cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是()
cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是()
| A.平衡正移 | B.(a+b)>(c+d) |
| C.Z的体积分数变小 | D.X的转化率变大 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间的变化曲线如图,下列表述中正确的是()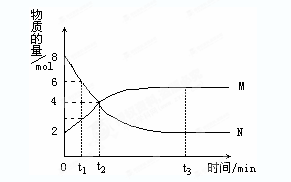
A.反应的化学方程式为:2M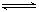 N N |
B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 | D.t1时,N的浓度是M浓度的2倍 |