已知A2+、B+、C3—、D— 是第三周期元素的四种离子。下列叙述中正确的是
A.四种离子都具有相同的电子层结构
B.原子半径:r(D)> r(C)> r(A)> r(B)
C.离子半径:r(B+)> r(A2+)> r(C3—)> r(D—)
D.B、D两元素的最高价氧化物的水化物在溶液中反应的离子方程式可表示为H++OH—=H2O
常温下,一定浓度的某溶液,由水电离出的c(OH-)=10-4mol/L,则该溶液中的溶质可能是()
| A.Al2(SO4)3 | B.CH3COONa | C.NaOH | D.KHSO4 |
已知25℃时,Ksp[Cu(OH)2]=2×10-20
(1)某CuSO4溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于________。
(2)要使0.2 mol·L-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为________。
已知同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2。就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是( )
A.Mg2++2HCO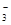 +2Ca2++4OH-===Mg(OH)2↓+2CaCO3↓+2H2O +2Ca2++4OH-===Mg(OH)2↓+2CaCO3↓+2H2O |
| B.Cu2++H2S===CuS↓+2H+ |
| C.Zn2++S2-+2H2O===Zn(OH)2↓+H2S↑ |
| D.FeS+2H+===Fe2++H2S↑ |
已知25℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol·L-1 HF溶液中加入1 L 0.2 mol·L-1 CaCl2溶液,则下列说法中,正确的是( )
| A.25℃时,0.1 mol·L-1 HF溶液中pH=1 |
| B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.该体系中没有沉淀产生 |
| D.该体系中HF与CaCl2反应产生沉淀 |
在100 mL 0.01 mol·L-1 KCl溶液中,加入1 mL 0.01 mol· L-1 AgNO3溶液,下列说法正确的是(已知AgCl的Ksp=1.8×10-10)( )
| A.有AgCl沉淀析出 | B.无AgCl沉淀析出 |
| C.无法确定 | D.有沉淀但不是AgCl |