氧元素与多种元素具有亲和力,所形成化合物的种类很多。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为__________。氧元素与氟元素能形成OF2分子,该分子的空间构型为__________。
(2)根据等电子体原理,在NO2+中氮原子轨道杂化类型是__________;1 mol O22+中含有的π键数目为__________个。
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。Cr3+基态核外电子排布式为__________。
(4)下列物质的分子与O3分子的结构最相似的是__________。
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(5)O3分子是否为极性分子?__________。
某溶液由盐酸、Na2CO3、H2SO4、CuCl2四种物质中的一种或几种混合形成,现向该混合溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示。
(1)该溶液中一定含 。(填化学式)
(2)写出图中a点之前的离子方程式: ;
写出图中a→b点的离子方程式: 。
(3)将所得沉淀进行过滤,洗涤,干燥,称量,应如何判断沉淀是否完全洗净:
。
(4)若b点时沉淀质量=2.94克,V1=20mL,V2=40mL,求C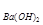 = 。
= 。
(1)若a克某气体中含有的分子数为b,则c克该气体在标准状况下的体积是(用NA表示阿伏加德罗常数)
(2)若同温同压下,m克A气体与n克B气体的分子数相同,则气体A与B在标况下的密度之比为 ,同质量的气体A与B的分子数之比为 。
(3)若以24克12C中所含的碳原子数为阿伏加德罗常数,则下列数值如何变化:(填“增大”、“减小”或“不变”)
O2的摩尔体积 ;O2的摩尔质量 ;同温同压下,一定质量O2的体积 ;同温同压下,一定体积O2的分子个数 。
有以下物质:
①石墨;②铝;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;
⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩氯化氢气体。
(1)其中能导电的是 ;属于非电解质的是 ;
属于强电解质的是 ;属于弱电解质的是 。
(2)写出物质⑥溶于水的电离方程式: 。
(3)写出物质⑥和⑧在水中反应的离子方程式: 。
(4)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式: 。
① 44.8L某气体在标准状况下的质量为142g,该气体的摩尔质量为_________;
② N2在标准状况下的密度为__________g/L;
③在mol AL2(SO4)3中含0.3molSO42—,其中含Al3+个。
①铁片;②饱和食盐水;③液态的纯硫酸;④蔗糖;⑤干冰;⑥熔融硝酸钾;⑦碳酸钙固体;⑧苛性钠;⑨氧化钠。用序号回答:
能导电的是______________,属于电解质的是____________,属于非电解质的是___________________。