茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是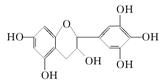
①分子式为C15H14O7
②1 mol儿茶素A在一定条件下最多能与7 mol H2加成
③等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应消耗金属钠和氢氧化钠的物质的量之比为1∶1
④1 mol儿茶素A与足量的浓溴水反应,最多消耗Br2 4 mol
| A.①② | B.②③ | C.③④ | D.①④ |
常温下,将浓度为0.1mol﹒L-1HCOOH的溶液加水不断稀释,下列各量始终保持增大的是
| A.c(H+) | B.Ka(HCOOH) | C.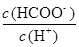 |
D.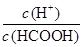 |
25℃,向纯水中加入少量的冰醋酸,有关该溶液的说法错误的是
| A.酸性增强 |
| B.c(H+)和c(OH-)的乘积增大 |
| C.pH减小 |
| D.c(OH-)减小 |
Mg(OH)2固体在水中存在下列溶解平衡:Mg(OH)2(s) 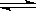 Mg2+(aq)+2OH-(aq),欲减少Mg(OH)2固体的量,可以加入少量的
Mg2+(aq)+2OH-(aq),欲减少Mg(OH)2固体的量,可以加入少量的
| A.NaOH固体 | B.NaCl固体 |
| C.MgSO4固体 | D.NaHSO4固体 |
下列实验符合要求的是
| A.滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 |
| B.用托盘天平称取NaOH固体时需先在左右两盘中各放上大小相同的纸片 |
| C.若25 mL滴定管中液面的位置在刻度为10mL处,则滴定管中液体的体积一定大于15 mL |
| D.用玻璃棒蘸取溶液滴在表面皿上的已润湿pH试纸上测得其pH为12 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.澄清透明的溶液中:K+、SO42﹣、Cu2+、Cl﹣ |
| B.0.1mol/L 的FeCl2的溶液中:H+、Na+、NO3﹣、Cl﹣ |
| C.使甲基橙变红的溶液中:K+、HCO3﹣、Ba2+、I﹣ |
| D.c(H+)/c(OH﹣)=1×10﹣12:NH4+、Cl﹣、Ca2+、Br﹣ |