国际无机化学命名委员会在1989年做出决定,把长式元素周期表原先的主副族及族号取消,由左至右改为18列。如碱金属为第1列,稀有气体元素为第18列。按此规定,下列说法中错误的是
| A.第9列元素中没有非金属元素 |
| B.第17列为卤族元素 |
| C.只有第2列元素原子的最外层有2个电子 |
| D.在整个18列元素中,第3列元素种类最多 |
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl一、NO3-、SO42-、CO32-。已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加人氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
回答下列问题:
(1)五种盐中,一定没有的阳离子是;所含的阴离子相同的两种盐的化学式是。
(2)D的化学式为,D溶液显碱性原因是(用离子方程式表示)。
(3)A和C的溶液反应的离子方程式是:;E和氨水反应的离子方程式是:。
(4)若要检验B中所含的阳离子,正确的实验方法是。
碱性锌锰电池的总反应为:Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH),下列说法不正确的是()
| A.该电池Zn为负极,MnO2为正极,电解质是KOH |
| B.放电时外电路电流由Zn流向MnO2 |
| C.电池工作时OH-向锌电极移动 |
| D.该电池的正极反应为:MnO2+e-+H2O=MnO(OH)+OH— |
短周期主族元素A、B、C的原子序数依次递增,它们的族序数之和为11,A、C同主族,B原子最外层电子数比A原子次外层电子数多l。下列叙述正确的是()
A.原子半径:B>C>A
B.A、C两元素的最高价氧化物对应水化物的酸性A弱于C
C.B的最高价氧化物的水化物只能与酸反应,不能与碱反应
D.B的最高价氧化物的熔点比A的最高价氧化物的熔点低
关于下列各实验装置的叙述中,正确的是()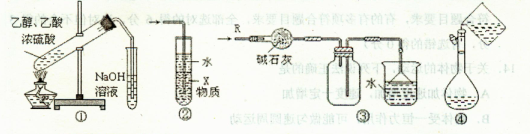
| A.装置①制备乙酸乙酯 |
| B.装置②中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| C.装置③可用于干燥、收集Cl2,并吸收多余的Cl2 |
| D.装置④配制一定物质的量浓度的溶液时转移液体 |
下列说法不正确的是()
| A.甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 |
| B.蔗糖、麦芽糖的分子式都是C12H22O1l,二者都属于低聚糖 |
| C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH |
| D.等质量的丙醇和乙酸完全燃烧时所需氧气的质量相同 |