若溶液中由水电离产生的c(OH-)=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是
| A.Al3+ Na+NO3- Cl- |
| B.K+ Na+Cl- NO3- |
| C.K+Na+ Cl-AlO2- |
| D.K+ NH4+ SO42-NO3- |
可逆反应:2NO2(g) 2NO(g)+ O2(g) 在体积不变的密闭容器中进行,达到平衡状态的标志是()
2NO(g)+ O2(g) 在体积不变的密闭容器中进行,达到平衡状态的标志是()
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
| A.①④ | B.②③⑤ | C.①③④ | D.①②③④⑤ |
下列离子方程式与所述事实相符且正确的是()
| A.用硫氰化钾溶液检验溶液中的Fe3+: Fe3++3SCN-=Fe(SCN)3↓ |
| B.钢铁生锈的负极电极反应: Fe —3e—= Fe3+ |
| C.证明氯气氧化性大于硫可用: Cl2+S2-=2Cl-+S↓ |
| D.用钠与硫酸铜溶液反应证明钠的金属性更强: 2Na+Cu2+=Cu+2Na+ |
设NA代表阿伏加德罗常数的数值,下列说法中正确的是()
| A.标准状况时,22.4L四氯化碳所含有的分子数为NA |
| B.34g H2O2中含有的非极性共价键数为 NA |
| C.碱性锌锰电池中,当有1.3g的锌消耗,则转移的电子数为0.002NA |
| D.将16gO2与64gSO2在一定的条件下充分反应生成的SO3分子数为NA |
下列既属于氧化还原反应,又属于吸热反应的是( )
| A.铝片与稀盐酸反应 | B.Ba(OH)2·8H2O与NH4Cl的反应 |
| C.灼热的炭与水蒸气的反应 | D.甲烷(CH4)在O2中的燃烧反应 |
下列化学用语书写正确的是()
| A.次氯酸的结构式:H-Cl-O |
B.氯化镁的电子式: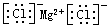 |
| C.作为相对原子质量测定标准的碳核素: 614C |
D.用电子式表示氯化氢分子的形成过程: |