(12分)如下图所示,A、B、C三个装置的烧杯中分别盛有足量的CuCl2溶液。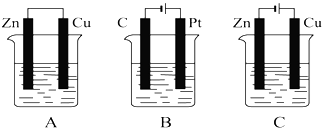
(1)A、B、C三个装置中属于原电池的是 属于电解池的是_____________。
(2)A池中Zn是_____________极,Cu极发生_____________(填“氧化”或“还原”)反应,电极反应为______ _______。反应过程溶液中c(Cu2+)___________(填“变大”“变小”或“不变”)。
(3)B池中C棒是 极,一段时间后的现象为 ,电极反应为_____ ____。B 池中的总反应为_ __。
(4)C池在化学反应中发生的能量转化形式是 。
碱存在下,卤代烃与醇反应生成醚(R—O—R′):
化合物A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下: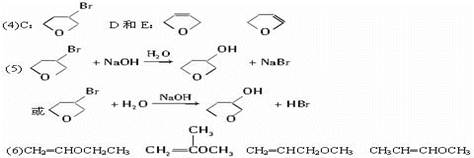
请完成下列问题:
(1)1 mol A和1 mol H2在一定条件下恰好反应,生成饱和一元醇Y,Y中碳元素的质量分数为65%,则Y的分子式为________________,A分子中所含官能团的名称是_______________,A的结构简式为_______________。
(2)第①②步反应类型分别为①_______________,②_______________。
(3)化合物B具有的化学性质(填写字母代号)是_______________。
a.可发生氧化反应
b.强酸或强碱条件下均可发生消去反应
c.可发生酯化反应
d.催化条件下可发生加聚反应
(4)写出C、D和E的结构简式:
C_____________、D和E______________________________。
(5)写出化合物C与NaOH水溶液反应的化学方程式:_______________________________。
(6)写出四氢呋喃链状醚类的所有同分异构体的结构简式:____________________________。
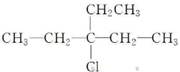
下列卤代烃在NaOH的醇溶液中加热得到的烯烃分别有几种?
(1)
(2)
已知卤代烃和NaOH的醇溶液共热可以得到烯烃,如: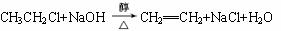
现通过以下步骤由 制取
制取 ,其合成流程如下:
,其合成流程如下: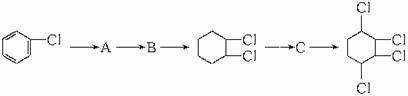
请回答下列问题:
(1)从左向右依次填写每步所属的反应类型是(a.取代反应 b.加成反应 c.消去反应)__________(只填写字母)。
(2)写出A B所需的试剂和反应条件。
B所需的试剂和反应条件。
石墨在加热和高压的条件下可加工成金刚石,这个变化是_____________(物理、化学)变化。