工业上制备纯硅时反应的热化学方程式为:SiCl4(g)+2H2(g)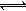 Si(s)+4HCl(g);△H=+QkJ/mol(Q>0),在相同的温度、压强条件下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
Si(s)+4HCl(g);△H=+QkJ/mol(Q>0),在相同的温度、压强条件下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
| A.反应过程中,若减小压强会降低SiCl4的转化率 |
| B.若反应开始时SiCl4为1mol,则达到反应平衡时,吸收的热量为QkJ |
C.反应至4min时,若HCl浓度为0.12mol/L,则H2的反应速率为0.03mol/(L min) min) |
| D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好完全反应 |
将0.01molNaOH和0.01mol Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的 关系的是
关系的是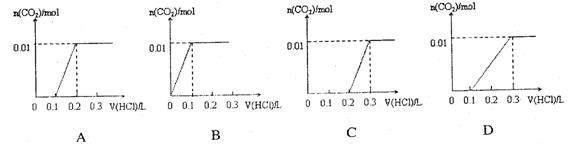
下列离子方程式正确的是
| A.向盐酸中滴加氨水:H++OH-=H2O |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C.碳酸氢钠溶液中通入少量SO2:2HCO3-+SO2=SO32-+2CO2↑+H2O |
| D.Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ |
W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7︰17;X与W 同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
| A.金属性:Y>Z | B.氢化物的沸点:X<W |
| C.离子的还原性:X<W | D.原子及离子半径:Z>Y>X |
有关实验的叙述,正确的是
A.将固体加入容量瓶中溶解并稀释至刻度,配置成一定物质的量浓度的溶液 |
B.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
C.用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
D.读取滴定管内液体的体积,俯视读数导致读数偏小 |
下 列判断错误的是
列判断错误的是
A.沸点 :
: B.熔点:Si>Al>Mg>Cl2>Ar
B.熔点:Si>Al>Mg>Cl2>Ar
C.酸性: C.碱性:
C.碱性: