由硝酸尾气的处理原理:3NO2+H2O ="=" 2HNO3+NO,NO2+NO+2NaOH ="=2" HNO2+ H2O,下列气体中,不可能被过量NaOH溶液完全吸收的是
| A.V(NO2): V(O2)= 4 : 1 |
| B.V(NO2): V(NO)= 1 : 0 |
| C.V(NO2): V(NO)= 1 : 2 |
| D.V(NO2): V(NO): V(O2)=" 1" : 1 : 1 |
下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是()
| A.氢氧化钠和硫酸铝 | B.氢氧化钠和氯化镁 |
| C.硫酸钠和氧氧化钡 | D.氯化铝和氨水 |
下列离子方程式书写正确的是()
A.NaHCO3溶液中加入少量NaHSO4溶液:HCO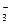 +HSO +HSO =SO =SO +H2O +H2O |
B.Ca(HCO3)2溶液中辊入少量Ca(OH)2溶液:Ca2++OH-+HCO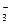 =CaCO3↓+H2O =CaCO3↓+H2O |
C.金属铝溶于氧化钠溶液:2Al+6OH-=2AlO +3H2↑ +3H2↑ |
| D.Fel2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3+=2Cl- |
下列有关工业生产的叙述正确的是()
| A.合成氮生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 |
| C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
| D.电解精练铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 |
关于下列反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4说法正确的是()
A.Cu2 S既是氧化产物又是还原产物 S既是氧化产物又是还原产物 |
B.产物中的SO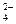 有一部分是氧化产物 有一部分是氧化产物 |
| C.5 mol FeS2发生反应,有10 mol电子转移 |
| D.FeS2只剩还原剂 |
菜温度下将氯气通入氢氧化钾溶液里,反应后得到KCI、KClO、KClO3的混合溶液。经测定ClO和ClO3的浓度之比为11:l,则氯气和氢氧化钾溶液反应时,被还原的氯元素和被氯化的氧元素的物质 的量之比为()
的量之比为()
A.1:3 B.4:3 C.2:l D .3:l
.3:l