用标准盐酸滴定未知浓度的NaOH溶液,如果测得结果偏低,则产生误差的原因可能是
| A.滴定过程中,锥形瓶中有溶液溅出 |
| B.锥形瓶用蒸馏水洗净后,未经干燥即进行滴定 |
| C.酸式滴定管未用标准盐酸润洗 |
| D.滴定前酸式滴定管尖嘴部分有气泡,滴定终止时气泡消失 |
1mol液态有机物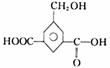 分别与足量
分别与足量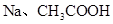 溶液、
溶液、 溶液反应,消耗三种药品的物质的量之比为
溶液反应,消耗三种药品的物质的量之比为
| A.3:2:1 | B.3:1:1 | C.3:1:2 | D.2:3:1 |
苯的结构式可用 来表示,下列关于苯的叙述中正确的是()
来表示,下列关于苯的叙述中正确的是()
| A.苯主要是以石油为原料而获得的一种重要化工原料 |
| B.苯中含有碳碳双键,所以苯属于烯烃 |
| C.苯分子中6个碳碳化学键完全相同 |
| D.苯可以与溴水、高锰酸钾溶液反应而使它们褪色 |
同温同压下,氦气、氢气和氨气的体积比为3∶2∶1,则其原子个数比为
| A.1∶2∶3 | B.4∶3∶3 | C.3∶4∶4 | D.3∶2∶1 |
关于吸热反应和放热反应下列说法中错误的是
| A.化学反应中的能量变化除了热量外还可以是光能、电能等 |
| B.需要加热才能进行的化学反应一定是吸热反应 |
| C.化学反应过程中的能量变化服从能量守恒定律 |
| D.生成物的总能量小于反应物的总能量时发生的是放热反应 |
《中华人民共和国食品安全法》于2009年1月1日起实施。下列做法不利于食品安全的是()
| A.用聚氯乙烯塑料袋包装食品 |
| B.在食盐中添加适量的碘酸钾 |
| C.在食品加工中科学使用食品添加剂 |
| D.研发高效低毒的农药,降低蔬菜的农药残留量 |