Na2O和Na2O2的下列叙述中正确的是
| A.Na2O比Na2O2稳定 | B.均可与水反应 |
| C.均可与CO2反应 | D.均是典型的碱性氧化物 |
下列各组离子在溶液中能大量共存的为()
| A.Cu2+、Fe3+、SCN-、K+ | B.Ba2+、AlO2-、OH-、Na+ |
| C.Cl-、H+、Na+、SO32- | D.ClO-、Na+、 Fe2+、 H+ |
下列物质反应后,产物与反应物的量无关的是()
| A.二氧化碳与石灰水 | B.盐酸与偏铝酸钠溶液 |
| C.铝单质和氢氧化钠溶液 | D.硫酸铝和氢氧化钡溶液 |
将一定量的NaHCO3和Na2CO3的混合物加热到不再放出气体时,收集到CO2 aL,待冷却后。向残余物中加入足量盐酸又收集到CO22aL(体积均在标准状况下测定)。则混合物中Na2CO3和NaHCO3的物质的量之比为()
| A.1∶1 | B.1∶2 | C.1∶3 | D.1∶4 |
能正确表示下列化学反应的离子方程式是( )
| A.SO2通入少量的氢氧化钠溶液: SO2 + OH- = HSO3- |
| B.NaAlO2和过量的盐酸:AlO2- + H+ + H2O = Al(OH)3↓ |
| C.铝片跟氢氧化钠溶液反应:2Al + 2OH- + H2O = 2AlO2- + 2H2↑ |
| D.氢氧化钡溶液与过量的小苏打的反应OH- +Ba2+ + HCO3- ═ BaCO3↓ + H2O |
现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液的体积关系如图所示,原溶液中Cl- 与SO42- 的物质的量之比为()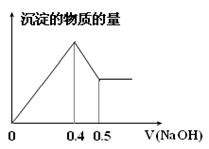
| A.1 :3 | B.2 :3 | C.6 :1 | D.3 :1 |