参照反应Br+H2―→HBr+H的能量对反应历程的示意图,下列叙述中正确的是
| A.正反应为吸热反应 |
| B.正反应为放热反应 |
| C.加入催化剂,该化学反应的反应热增大 |
| D.从图中可看出,该反应的反应热与反应途径有关 |
与pH类似,我们定义pOH=-lgc(OH-),下列溶液,一定呈中性的是
| A.c(H+)=1×10-7mol·L-1的溶液 | B.水电离的H+和OH-浓度相等的溶液 |
| C.pH+pOH=14的溶液 | D.pH=pOH的溶液 |
在密闭容器中进行以下可逆反应:A(g)+B(g)  C(g)+2D(?),在不同的条件下C的百分含量的变化情况如图,则该反应描述正确的是
C(g)+2D(?),在不同的条件下C的百分含量的变化情况如图,则该反应描述正确的是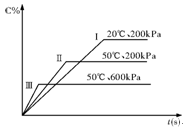
| A.正反应放热,D是固体 |
| B.正反应放热,D是气体 |
| C.正反应吸热,D是气体 |
| D.正反应放热,D是固体或气体 |
如图是关于N2+3H2 2NH3 ΔH<0的速率—时间图象,则t1时刻使平衡发生移动的原因是
2NH3 ΔH<0的速率—时间图象,则t1时刻使平衡发生移动的原因是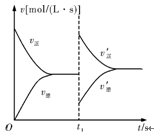
| A.升高温度,同时增大压强 |
| B.降低温度,同时减小压强 |
| C.增大反应物的浓度,同时使用适宜的催化剂 |
| D.增大反应物的浓度,同时减小生成物的浓度 |
W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y。下列说法正确的是
| A.Y的低价氧化物与O3漂白的原理相同 |
| B.Y的氢化物和W2Y所含化学键的类型相同 |
| C.上述三种元素形成的简单离子,X离子半径最小 |
| D.工业上常用电解相应的盐溶液制备W、X的单质 |
某氨水的pH=a,某盐酸的pH=b,已知a+b=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是
A.c(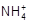 )>c(Cl-)>c(H+)>c(OH-) )>c(Cl-)>c(H+)>c(OH-) |
B.c(Cl-)>c(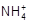 )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
C.c(Cl-)>c(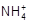 )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
D.c(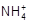 )+c(H+)=c(Cl-)+c(OH-) )+c(H+)=c(Cl-)+c(OH-) |