为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是
| 编 号 |
被提纯的物质 |
除杂试剂 |
分离方法 |
| A |
己烷(己烯) |
溴水 |
分液 |
| B |
淀粉溶液(NaCl) |
水 |
过滤 |
| C |
甲烷(乙烯) |
酸性高锰酸钾溶液 |
洗气 |
| D |
苯(苯酚) |
NaOH溶液 |
分液 |
某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是()
A.K+、Na+、HCO 、NO 、NO |
B.Na+、SO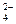 、Cl—、ClO— 、Cl—、ClO— |
C.H+、Mg2+、SO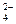 、NO 、NO |
D.Ag+、K+、NO 、Na+ 、Na+ |
设NA为阿伏伽德罗常数,下列叙述正确的是 ()
()
| A.24g镁的原子量最外层电子数为NA | |
B.1L0.1mol·L-1乙酸溶液中H+数为0.1NA |
C.1mol甲烷分子所含质子数为10NA |
| D.标准状况下,22.4L乙醇的分子数为NA |
NA为阿伏伽德罗常数,下列叙述错误的是()
| A.18gH2O中含的质子数为10NA |
| B.12g金刚石含有的共价键数为4NA |
| C.46gNO2和N2O4混合气体中含有原子总数为3NA |
| D.1 mol Na 与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
短周期元素甲和乙,甲原子的最外层电子数为a,次外层电子数为b;乙原子的M层电子数为(a – b – 1),L层电子数为(a + b)。则甲、乙两元素形成的化合物具有的性质是
①与水反应②与硫酸反应③与氢氧化钠溶液反应④与氯气反应
| A.①② | B.②③ | C.②④ | D.③④ |
下列有关杂化轨道的说法中错误的是
| A.ⅠA族元素成键时不可能有杂化轨道 |
| B.s轨道和p轨道不可能有sp4出现 |
| C.杂化轨道既可能形成σ键,也可能形成π键 |
| D.孤对电子有可能参加杂化 |