100℃时, 。下列三种溶液:①0.001 mol·L-1氨水与0.001 mol·L-1HCl溶液等体积混合液②pH=3的HCl与pH=11的NaOH溶液等体积混合液 ③pH=11的氨水与pH=1的HCl溶液等体积混合液。其中呈酸性的是
。下列三种溶液:①0.001 mol·L-1氨水与0.001 mol·L-1HCl溶液等体积混合液②pH=3的HCl与pH=11的NaOH溶液等体积混合液 ③pH=11的氨水与pH=1的HCl溶液等体积混合液。其中呈酸性的是
| A.① | B.③ | C.②③ | D.①③ |
如果4g甲烷含有的分子数为a个,则阿伏加德罗常数用含a的代数式可表示为()
| A.a mol-1 | B.0.25amol-1 | C.2amol-1 | D.4amol-1 |
已知3.01×1023个X气体分子的质量为16g,则X气体的摩尔质量是()
| A.16g | B.32g | C.64g /mol | D.32g /mol |
下列各组物质,前者是单质,后者为混合物的是()
| A.石墨、冰水混合物 | B.铁粉、食醋 |
| C.碘酒、食盐 | D.盐酸、空气 |
下列叙述正确的是()
| A.1 mol H2O的质量为18g/mol |
| B.CH4的摩尔质量为16g |
| C.3.01×1023个SO2分子的质量为32g |
| D.标准状况下,1 mol任何物质的体积都约为22.4L |
下列反应不属于四种基本反应类型,但属于氧化还原反应的是()
| A.Fe+CuSO4=FeSO4+Cu |
B.3CO+Fe2O3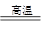 2Fe+3CO2 2Fe+3CO2 |
| C.AgNO3+NaCl=AgCl↓+NaNO3 |
D.2KMnO4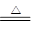 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |