短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法不正确的是
| A.元素W、X的氯化物中,各原子均满足8电子的稳定结构 |
| B.元素X与氢形成的原子个数比为1:4的化合物中只含有极性共价键 |
| C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 |
| D.元素Z可与元素X形成共价化合物XZ2 |
下列说法中正确的是( )
| A.在Na3PO4溶液中,c(Na+)是c(PO43-)的3倍 |
| B.pH为3的盐酸中,其c(H+)是pH为1的盐酸中c(H+)的3倍 |
| C.0.1 mol·L-1KOH溶液和0.1 mol·L-1氨水中,其c(OH-)相等 |
| D.在25℃时,无论是酸性、碱性还是中性的稀溶液中,其c(H+)和c(OH-)的乘积都等于1×10-14 |
通过对下图的观察,有以下几种叙述,其中不正确的是( )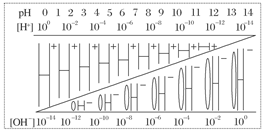
| A.该温度下,不论何种水溶液中c(H+)、c(OH-)乘积相等,即水的离子积是一个常数 |
| B.若醋酸钠溶液中c(Na+)=c(CH3COO-),则溶液中的c(H+)=c(OH-) |
| C.如果定义pOH=-lg c(OH-)时,则该温度下某水溶液中的pOH和pH之和等于14 |
| D.某水溶液由于条件的改变,如果氢离子浓度变小,则氢氧根离子浓度一定变大 |
下列叙述正确的是( )
| A.0.1 mol/L C6H5ONa溶液中:c(Na+)>c(C6H5O-)>c(H+)>c(OH-) |
| B.Na2CO3溶液加水稀释后,恢复至原温度,pH和KW均减小 |
| C.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 |
| D.在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降 |
25℃时,pH=13的氨水中由水电离出的c(H+)=a,pH=1的盐酸中由水电离出的c(H+)=b,0.2 mol·L-1盐酸与0.1 mol·L-1氢氧化钠溶液等体积混合后,由水电离出的c(H+)=c,则a、b、c的关系正确的是( )
| A.a>b=c | B.a=b=c |
| C.c>a=b | D.a>c>b |
下列物质按照纯净物、混合物、电解质和非电解质顺序排列的是( )
| A.盐酸、水煤气、醋酸、干冰 |
| B.冰醋酸、福尔马林、硫酸钠、乙醇 |
| C.单甘油酯、混甘油酯、苛性钠、氯气 |
| D.胆矾、漂白粉、氯化钾、氯气 |