(1)室温下,如果将0.1molCH3COONa和0.05molHCl全部溶于水,形成混合溶液(假设无损失), 和 两种粒子的物质的量之和等于0.1mol。
(2)已知某溶液中只有Na+、CH3COO-、H+、OH-四种离子。某同学推测该溶液中离子浓度可能有如下四种关系:
A.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.c(Na+)>c(CH3COO-)>c(H+) >c(OH-)
C.c(Na+)>c(OH-)> c(CH3COO-)>c(H+)
D.c(CH3COO-)>c(Na+)>c(H+) >c(OH-)
①若溶液中只溶解了一种溶质,该溶质的名称是 ,上述离子浓度大小关系中正确的是(填序号) ;
②若上述关系中D是正确的,则溶液中溶质的化学式是 ;
③若该溶液由体积相等的醋酸与NaOH溶液混合而成,且溶液恰好呈中性,则混合前c(CH3COOH)(填“>”“<”“=”,下同) c(NaOH),混合后c(CH3COO-)与c(Na+)的关系是c(CH3COO-) c(Na+)。
(3)25℃时,向0.1mol/L的醋酸溶液中加入少量的醋酸钠固体,当固体溶解后,测得溶液的pH增大,主要原因是 (填序号)
A.醋酸与醋酸钠发生反应
B.醋酸钠溶液水解显碱性,增加了c(OH-)
C.醋酸钠溶于水电离出醋酸根离子,抑制了醋酸的电离,使c(OH-)减小。
恒容容积为VL的密闭容器中发生2NO2 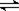 2NO+O2反应。反应过程中NO2的物质的量随时间变化的状况如图所示。
2NO+O2反应。反应过程中NO2的物质的量随时间变化的状况如图所示。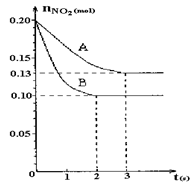
(1)若曲线A和B表示的是该反应在某不同条件下的反应状况,则该不同条件是。
A.有、无催化剂 B.温度不同 C.压强不同 D.体积不同
(2)写出该反应的化学平衡常数K的表达式:,并比较K800℃K850℃(填“>”、“<”或“=”)。
(3)求算在B条件下从反应开始至达到平衡,氧气的反应速率v(O2)=。
(4)不能说明该反应已达到平衡状态的是。
A.v正(NO2)=v逆(NO)B.c(NO2)=c(NO)
C.气体的平均摩尔质量不变 D.气体的密度保持不变
(5)在如图所示的三个容积相同的三个容器①、②、③进行反应:2NO+O2 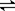 2NO2
2NO2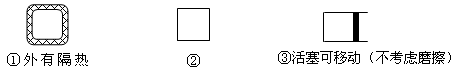
若起始温度相同,分别向三个容器中充入2molNO和1molO2 ,则达到平衡时各容器中NO物质的百分含量由大到小的顺序为(填容器编号)。
室温时,向1 L 0.01mol/L的硫酸氢钠溶液中,滴入等体积的0.01 mol/L的Ba(OH)2溶液后,加水稀释到10 L,所发生反应的离子方程式为______________________,此时溶液的pH=__________;若向1L0.1mol/L的NaHSO4溶液中逐滴加入1L0.1mol/L Ba(OH)2溶液至溶液呈中性,此时发生反应的离子方程式______________________。
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有5个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A的最高价氧化物对应的水化物是_______(填化学式);
(2)物质E中所包含的化学键有________,写出C、D两元素形成的化合物C2D的电子式_________;
(3)在同主族氢化物的递变性质中,A的氢化物沸点反常,这可以用解释。
A.共价键 B.离子键 C.氢键 D.范德华力
(4)与C同主族且处于第七周期的元素的原子序数是.
在一定条件下,向体积为2 L的容器中加入2 mol O2和3 mol SO2使之反应生成SO3气体:2SO2+ O2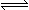 2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
2SO3,2 min时,测得O2的物质的量为1.6 mol,则:
(1)2min内,平均反应速率v(O2)=; v(SO3)=。
(2)2min时,SO2的浓度为
(3)若2min时测得上述反应放出Q kJ的热量,试写出该反应的热化学方程式
根据元素周期表,填写下列空白:
(1)最活泼的非金属元素位于周期表中第_____周期第族。某核素A含有8个质子、10个中子,A的核素符号是_____,原子结构示意图
(2)在第三周期中,A、B两元素的原子序数之差为4,它们组成化合物AB的电子式为______.
(3)1mol某物质含有不同周期的三种元素各1mol,其核电荷总数为20mol,该物质的化学式为_____;是化合物(离子或共价)