H2和I2在一定条件下能发生反应:H2(g)+I2(g) 2HI(g) ΔH=-a kJ·mol-1
2HI(g) ΔH=-a kJ·mol-1
已知: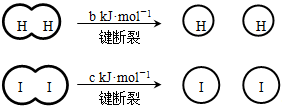
(a、b、c均大于零)
下列说法不正确的是
| A.反应物的总能量高于生成物的总能量 |
| B.断开1 mol H—H键和1 mol I—I键所需能量大于断开2 mol H—I键所需能量 |
| C.断开2 mol H—I键所需能量约为(c+b+a)kJ |
| D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.0.2 NA个氢分子的体积为4.48 L |
| B.常温常压下,5.85gNaCl中含有0.1NA个分子 |
| C.200mL 1 mol·L-1的Fe2(SO4)3溶液中Fe3+数小于0.4NA |
| D.1 molCl2与足量NaOH溶液充分反应,转移的电子数为2NA |
下列实验中,所采取的分离方法不正确的是
| 选项 |
目的 |
分离方法 |
| A |
提取NaCl溶液中的碘单质 |
乙醇萃取 |
| B |
分离乙酸乙酯和饱和Na2CO3溶液 |
分液 |
| C |
除去NaCl固体中的NH4Cl |
加热 |
| D |
除去Cl2中的HCl |
饱和食盐水洗气 |
下列有关实验操作的说法正确的是
| A.测定溶液pH时,用玻璃棒蘸取少量溶液点在湿润的pH试纸上再与标准比色卡比对 |
| B.过滤时,用玻璃棒搅拌漏斗中的液体以加快过滤速度 |
| C.做钠在氧气中燃烧实验时,用镊子从煤油中取出金属钠,直接放入坩锅中加热 |
| D.NaCl溶液蒸发结晶时,蒸发皿中有大量晶体析出时停止加热 |
下列反应的离子方程式正确的是
| A.往NaAlO2溶液中通入过量CO22AlO2-+ CO2 + 3H2O=2Al(OH)3↓ + CO32- |
| B.Na2SiO3溶液与稀醋酸混合 SiO32-+ 2H+=H2SiO3↓ |
| C.钠与CuSO4溶液反应 2Na + Cu2+=Cu + 2Na+ |
| D.往Na2SO3溶液中滴加双氧水 H2O2 + SO32-=SO42-+ H2O |
反应2X(g)+Y(s) 2Z(g) ΔH<0,达到平衡时,下列说法正确的是
2Z(g) ΔH<0,达到平衡时,下列说法正确的是
| A.减小容器体积,平衡不移动 |
| B.增大Y的量,Z的百分含量增大 |
| C.加入催化剂,X的转化率增大 |
| D.降低温度,正反应速率增大、逆反应速率减小 |