现有如下各种说法,正确的是
①在水中氢、氧原子间均以化学键相结合
②金属元素的原子和非金属元素的原子化合均形成离子键
③离子键是阴、阳离子的相互吸引力
④根据电离方程式HCl===H++Cl-,判断HCl分子中存在离子键
⑤H2分子和Cl2分子的反应过程是H2、Cl2分子中共价键发生断裂生成H、Cl原子,而后H、Cl原子形成离子键的过程
| A.①②⑤正确 | B.都不正确 |
| C.④正确,其他不正确 | D.仅①不正确 |
一定量的浓硝酸与过量的铜充分反应,生成的气体是()
| A.只有NO2 | B.只有NO | C.NO2和NO | D.NO2和H2 |
铋(Bi)在医药方面有重要应用。下列关于 Bi和
Bi和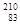 Bi的说法正确的是()
Bi的说法正确的是()
A. Bi和 Bi和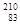 Bi都含有83个中子 Bi都含有83个中子 |
B. Bi和 Bi和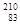 Bi互为同位素 Bi互为同位素 |
C. Bi和 Bi和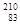 Bi的核外电子数不同 Bi的核外电子数不同 |
D. Bi和 Bi和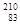 Bi分别含有126和127个质子 Bi分别含有126和127个质子 |
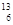 C-NMR(核磁共振)可以用于含碳化合物的结构分析,有关
C-NMR(核磁共振)可以用于含碳化合物的结构分析,有关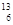 C的说法正确的是()
C的说法正确的是()
| A.质子数为6 | B.电子数为13 |
| C.中子数为6 | D.质量数为6 |
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
| A.取a克混合物充分加热,得b1克固体 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b2克固体 |
| C.取a克混合物与足量浓盐酸充分反应,逸出气体用碱石灰吸收,增重b3克 |
| D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b4克固体 |
下列各图所示的实验原理、方法、装置或操作正确的是