下列反应属于放热反应的是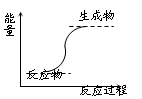
| A.氢氧化钡晶体和氯化铵晶体的反应 |
| B.能量变化如上图所示的反应 |
| C.化学键断裂吸收的热量比化学键生成放出的热量多的反应 |
| D.燃烧反应和酸碱中和反应 |
下列关于有机物的说法完全正确的是
| A.只有在生物体内才能合成的物质 | B.含有碳元素的物质 |
| C.有机化合物都能燃烧 | D.有机化合物都是含有碳元素的化合物 |
铋(Bi)在医药方面有重要应用。下列关于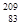 Bi和
Bi和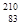 Bi的说法正确的是()
Bi的说法正确的是()
A.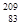 Bi和 Bi和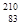 Bi的核外电子数不同 Bi的核外电子数不同 |
B.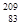 Bi和 Bi和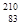 Bi分别含有126和127个质子 Bi分别含有126和127个质子 |
C.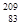 Bi和 Bi和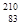 Bi互为同位素 Bi互为同位素 |
D.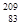 Bi和 Bi和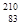 Bi都含有83个中子 Bi都含有83个中子 |
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是()
| A.分液、萃取、蒸馏 |
| B.萃取、蒸馏、分液 |
| C.分液、蒸馏、萃取 |
| D.蒸馏、萃取、分液 |
同温同压下,等质量的CO和CO2 气体相比较,下列叙述中正确的是()
| A.所含碳原子数比为1∶1 |
| B.体积比为1∶1 |
| C.密度比为7∶11 |
| D.分子数比为7∶11 |
下列鉴别物质的方法能达到目的是()
| A.用加热、称重的方法鉴别Na2CO3固体和NaHCO3固体 |
| B.用焰色反应鉴别NaCl固体和NaOH固体 |
| C.某溶液中滴加盐酸能产生无色气体,该气体能使澄清石灰水变浑浊,则原溶液中一定含CO32﹣ |
| D.向某溶液中加入BaCl2溶液出现白色沉淀,再加入HCl溶液,白色沉淀不溶解,则该溶液中肯定有SO42 |