下列说法中正确的是
| A.氯化氢溶于水能电离出H+、Cl—,所以氯化氢是离子化合物 |
| B.碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子之间的作用力 |
| C.烧碱固体溶于水的过程中,共价键被破坏 |
| D.有机化合物CH3CH2NO2与H2N—CH2—COOH是同分异构体 |
用图甲所示装置进行实验,若图乙中横坐标x表示流入电极的电子的物质的量。下列叙述不正确的是( )
| A.E表示反应生成Cu的物质的量 |
| B.E表示反应消耗H2O的物质的量 |
| C.F表示反应生成H2SO4的物质的量 |
| D.F表示反应生成O2的物质的量 |
某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是( )
| A.铅笔端作阳极,发生还原反应 |
| B.铂片端作阴极,发生氧化反应 |
| C.铅笔端有少量的氯气产生 |
| D.a点是负极,b点是正极 |
如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
| A.a为负极,b为正极 |
| B.a为阳极,b为阴极 |
| C.电解过程中,d电极质量增加 |
| D.电解过程中,氯离子浓度不变 |
如图所示,a、b是多孔石墨电极。某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两支玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转。下列说法不正确的是( )
| A.断开K2,闭合K1一段时间,溶液的pH变大 |
| B.断开K1,闭合K2时,b极上的电极反应为2H++2e-=H2↑ |
| C.断开K2,闭合K1时,a极上的电极反应为4OH--4e-=O2↑+2H2O |
| D.断开K1,闭合K2时,OH-向b极移动 |
如图是在待镀铁制品上镀铜的实验装置,则下列说法正确的是( )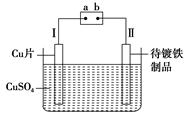
| A.电源a极为负极 |
| B.Ⅰ极上铜放电而逐渐消耗 |
| C.Ⅱ极上发生的电极反应为Fe-2e-=Fe2+ |
| D.Ⅱ极上Cu2+放电而使溶液中Cu2+浓度逐渐变小 |