一定量的有机物溶解于适量的NaOH溶液中,滴入酚酞试液呈红色,煮沸5 min后,溶液颜色变浅,再加入盐酸显酸性后,沉淀出白色晶体;取少量晶体放到FeCl3溶液中,溶液又呈紫色,则该有机物可能是
A.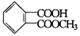 |
B.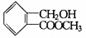 |
C. |
D. |
下列叙述能证明次氯酸是一种弱酸的是( )
| A.次氯酸不稳定,易分解 |
| B.次氯酸是一种强氧化剂 |
| C.次氯酸钙能与碳酸作用生成碳酸钙和次氯酸 |
| D.次氯酸能使染料和有机色质褪色 |
自来水一般是用少量的氯气消毒。如果实验室中临时没有蒸馏水,可以用自来水配制某些急需的药品,但有些药品若用自来水配制,则明显会导致药品变质。下列哪些药品不能用自来水配制( )
| A.Na2SO4 |
| B.NaCl |
| C.AgNO3 |
| D.K2CO3 |
两只烧杯中各加入相同体积的3 mol·L-1的稀硫酸置于天平左右两个托盘上,天平平衡,向一个烧杯中加入10.8 g Al,向另一烧杯中加入10.8 g Fe,反应完毕后,下列叙述正确的是( )
| A.若天平倾斜,有可能放Al的一端托盘上升 |
| B.若天平倾斜,一定是放Al的一端托盘上升 |
| C.若天平倾斜,有可能是放Fe的一端上升 |
| D.有可能天平两端仍保持平衡 |
将等量的小苏打用下列两种方法制取CO2:甲法——加热,乙法——跟足量的酸反应。两种方法得到的CO2气体的量的关系为( )
| A.甲法多 | B.乙法多 | C.一样多 | D.无法比较 |
下列离子方程式错误的是( )
A.铝粉投入到NaOH溶液中2Al+2OH-====2 +2H2O +2H2O |
B.Al(OH)3溶于NaOH溶液Al(OH)3+OH-==== +2H2O +2H2O |
| C.Al(OH)3溶于HCl溶液Al(OH)3+3H+====Al3++3H2O |
D.Al2O3粉末溶于NaOH溶液Al2O3+2OH-====2 +H2O +H2O |