利用人工模拟光合作用合成甲酸的原理为:
2CO2+2H2O 2HCOOH+O2,装置如图所示,
2HCOOH+O2,装置如图所示,
下列说法不正确的是
| A.电极1周围pH增大 |
| B.电子由电极1经过负载流向电极2 |
| C.电极2的反应式:CO2+2H++2e-=HCOOH |
| D.该装置能将太阳能转化为化学能和电能 |
下列实验操作或说法,正确的是()
| A.向盛水的烧杯中投入一大块钠,这样现象更明显 |
B.钠也可以保存在CCl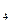 中 中 |
| C.将一小块钠放在石棉网上加热,观察现象 |
| D.钠很软,可用手掰开来观察它的颜色 |
将9.2 g金属钠投入到100 g下列不同质量分数的盐酸中,则放出的氢气()
①2.00%②3.65%③10%④36.5%
| A.①最少 | B.④最多 | C.③居中 | D.一样多 |
电子工业制造光电管时,需要一种经强光照射就失去电子,从而接通电路的材料。制造这种材料的物质应该是()
| A.放射性元素 | B.超铀元素 |
| C.活泼非金属元素 | D.碱金属元素 |
关于某溶液所含离子检验的方法和结论正确的是()
A.加入过量NaOH溶液,有白色沉淀生成,则原溶液一定有Mg |
B.加入AgNO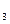 溶液有白色沉淀生成,加稀盐酸沉淀不消失,则原溶液一定有Cl 溶液有白色沉淀生成,加稀盐酸沉淀不消失,则原溶液一定有Cl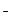 |
C.加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中可能有CO 或SO 或SO |
| D.加入NaOH并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液是铵盐溶液 |
若将2.3 g金属钠试样置于过量O 中燃烧后,生成了3.6 g固体物质,则下列推断合理的是()
中燃烧后,生成了3.6 g固体物质,则下列推断合理的是()
| A.钠在燃烧前已有部分氧化变质 |
| B.钠在燃烧前未氧化变质 |
| C.无法确定钠在燃烧前是否已氧化变质 |
| D.燃烧产物中只有氧化钠 |