石墨炔是由1,3-二炔键与苯环形成的平面网状结构的全碳分子,具有优良的化学稳定性和半导体性能。下列关于石墨炔的说法不正确的是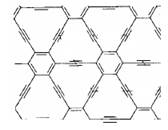
| A.石墨炔属于芳香烃 |
| B.石墨炔与金刚石互为同素异形体 |
| C.石墨炔有望代替半导体材料硅在电子产品中得到广泛应用 |
| D.石墨炔孔径略大于H2分子的直径,因此它是理想的H2提纯薄膜 |
下列各项叙述中,正确的是
A Ge的电负性为1.8,则其是典型的非金属
B L层不含s能级,M层存在3f能级
C焰火是焰色反应,都是电子由基态跃迁到激发态的结果
D在电子云示意图中,小黑点是电子在原子核外出现的概率密度的形象描述
下列说法正确的是()
| A.基态时相同周期的两种元素的原子所占用的能级和能层是一样的 |
| B.基态时稀有气体元素原子的价层电子数都为8 |
| C.基态时同种元素的原子和离子的轨道排布式一样 |
| D.非金属元素原子的d轨道一定不填充电子或填满电子 |
下列各元素原子排列中,其电负性减小顺序正确的是( )
| A.K>Na>Li | B.F>O>S | C.P>Mg>Al | D.C>N>O |
下列说法正确的是( )
| A.SiH4比CH4稳定 |
| B.O2-半径比F-的小 |
| C.P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的弱 |
| D.Na和Rb属于第ⅠA族元素,Rb失电子能力比Na的强 |
下列各项叙述中,正确的是
| A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| B.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是S区元素 |
| C.所有原子任一能层的S电子云轮廓图都是球形,但球的半径大小不同 |
| D.24Cr原子的电子排布式是:1s22s22p63s23p63d44s2 |