设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.在Cl2与NaOH溶液的反应中,每0.1molCl2参加反应时,转移电子的数目为0.2NA |
B.0.1mol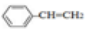 中含有双键的数目为0.4NA 中含有双键的数目为0.4NA |
| C.标准状况下,11.2L乙醇中含有羟基的数目为0.5NA |
| D.4.6g由NO2和N2O4组成的混合物中含有氧原子的数目为0.2NA |
在一定温度下,可逆反应A(g)+3B(g) 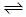 2C(g) 达到平衡状态的标志是
2C(g) 达到平衡状态的标志是
A.生成的速率与A分解的速率相等
B.单位时间生成nmolA,同时生成3nmolB
C.A、B、C的浓度不再变化
D.A、B、C的分子数比为1:3:2
在2A+B  3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.v(A)=0.5 mol·L-1·s-1B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1D.v(D)=1 mol·L-1·s-1
已知298K时,H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ•mol﹣1,推测含1mol HCl的稀溶液与含1mol NH3的稀溶液反应放出的热量
| A.小于57.3 kJ | B.等于57.3 kJ | C.大于57.3kJ | D.无法确定 |
25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
A.2H2(g)+O2(g) ="=" 2H2O(1)△H= ―285.8kJ/mol |
| B.2H2(g)+ O2(g) ="=" 2H2O(1)△H= +571.6 kJ/mol |
| C.2H2(g)+O2(g) ="=" 2H2O(g)△H= ―571.6 kJ/mol |
D.H2(g)+ O2(g) ="=" H2O(1)△H= ―285.8kJ/mol O2(g) ="=" H2O(1)△H= ―285.8kJ/mol |
下列各图所表示的反应是吸热反应的是 