、
、
、
是初中化学常见的物质,在一定条件下四种物质存在如下图所示的转化关系:
。
(1)若
是硫酸,
是氢氧化钠,该反应的基本类型是
(2)若
、
均是含同种元素的非金属氧化物,且
有毒性,
能被磁铁吸引。
①
的化学式是
②
的合金可用于制作炊具,主要是利用它的
(3)若
、
是都是金属单质,
、
都是盐,请写出一个符合要求的化学方程式:
从海水中可制备纯碱和金属镁,其流程如图所示.
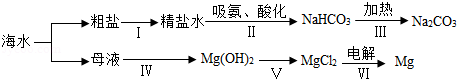
(1)粗盐提纯时,每步操作都会用到的一种玻璃仪器是 .(填仪器名称)
(2)粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质:a.适量的盐酸;b.稍过量的Na2CO3溶液;c.稍过量的Ba(OH)2溶液,利用过滤等操作进行除杂,则加入这三种物质的先后顺序为 .(填字母序号)
(3)向饱和的氯化钠溶液中通入氨气和二氧化碳,经过一系列变化,最终可得到纯碱.请写出第Ⅲ步反应的化学方程式 .
(4)第Ⅴ步Mg(OH)2与盐酸的反应 中和反应.(选填“是”或“不是”)
火力发电附近农作物产量急剧下降.经科技人员检测发现:附近雨水pH约为5.0,土壤pH约为5.4.已知一些主要农作物适宜生长的土壤pH如下:
|
农作物 |
玉米 |
小麦 |
马铃薯 |
|
pH |
6~7 |
6.3~7.5 |
4.8~5.5 |
(1)根据数据,该土壤最适合种植的农作物是 .
(2)要改良酸性土壤应选择一种适合的碱,这种碱是 .
(3)该地形成酸雨的主要原因是燃煤中产生的 .
人类的生活和生产都离不开金属.铝、铁、铜是人类广泛使用的三种金属,与我们的生活息息相关.
(1)生活中常用铜做导线,主要是利用了铜的 .
(2)铝制品具有良好抗腐蚀性能的原因是 .
(3)为了验证三种金属的活动性顺序,可选择Al、Cu和下列试剂中的 来达到实验目的.(选填字母序号)
A.Al 2(SO 4) 3溶液 B.FeSO 4溶液 C.CuSO 4溶液
(4)请你写出一条保护金属资源的有效途径 .
图1为甲、乙两种物质(均不含结晶水)的溶解度曲线图。请回答下列问题。
(1)在10℃时,甲的溶解度 乙的溶解度。(选填">""<"或"=")
(2)在20℃时,向盛有50g水的烧杯中加入25g甲物质,充分搅拌后溶液质量是 g。
(3)取乙进行如图2实验,属于饱和溶液的是 ,溶质质量分数最大的是 。

化学是一门以实验为基础的科学,在进行实验操作时,可能遇到突发情况,我们需要掌握一些应急处理的常识.
(1)若酒精灯内洒出的酒精在桌上燃烧起来,应该 灭火.
(2)为防止燃气泄露造成危险,在家中应该安装 .
(3)若不慎将浓硫酸沾在皮肤上,应现用大量水冲洗,然后再涂上3%~5%的 溶液.