有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生。
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。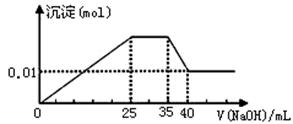
根据上述实验,以下推测不正确的是
| A.原溶液一定不存在H+、Cu2+、CO32- |
| B.不能确定原溶液是否含有K+、NO3- |
| C.实验所加的NaOH的浓度为2mol·L-1 |
| D.原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n( NH4+)=1:1: 2 |
A、B、C、D是含同一元素的四种物质,相互之间有如图的转化关系,其中A是单质,D是最高价氧化物的水化物。那么A可能是
A.SB.Cl2C.FeD.Si
下列有关化学用语使用正确的是
A.硫原子的原子结构示意图: |
B.NH4Cl的电子式: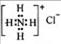 |
C.N2的结构式::N≡N: |
D.原子核内有10个中子的氧原子: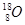 |
重水(D2O)是重要的核工业原料,下列说法错误的是
A.氘(D)原子核外有1个电子B.1H与D互称同位素
C.H2O与D2O互称同素异形体D.1H218O与D216O的相对分子质量相等
下列物质中,不能由单质直接化合生成的是
①CuS ②FeS ③SO3④H2S ⑤FeCl2
| A.①③⑤ | B.①②③⑤ | C.①②④⑤ | D.全部 |
 是重要的核工业原料,在自然界的存在很少。
是重要的核工业原料,在自然界的存在很少。 的浓缩一直为国际社会关注。下列有关
的浓缩一直为国际社会关注。下列有关 说法正确的是
说法正确的是
A. 原子核中含有92个中子 原子核中含有92个中子 |
B. 原子核外有143个电子 原子核外有143个电子 |
C. 与 与 互为同位素 互为同位素 |
D. 与 与 互为同素异形体 互为同素异形体 |