两种有机物A、B分子式均为C11H12O5,A或B在稀H2SO4中加热均能生成C和D。
已知:
①A、B、C、D能与NaHCO3反应;
②只有A、C能与FeCl3溶液发生显色反应,且核磁共振氢谱显示苯环上有两种不同化环境的氢原子;
③H能使溴水褪色且不含有甲基;
④F能发生银镜反应。
D能发生如下变化:
(1)D→H的反应类型______________________________,D中官能团名称________________________。
(2)写出C的结构简式____________________________________。
(3)D→G的化学方程式_____________________________________。
(4)B在NaOH溶液中受热的化学方程式 ____________________。
(5)C的同分异构体有多种,写出同时满足下列三个条件的同分异构体的结构简式:(任写一种)________________________。
① 苯环上一卤代物只有两种;
② 能与FeCl3溶液发生显色反应;
③ 能发生银镜反应。
结晶玫瑰是一种具有玫瑰香气的香料,可由下列方法合成(部分反应物及反应条件未标出):已知A是苯的一种同系物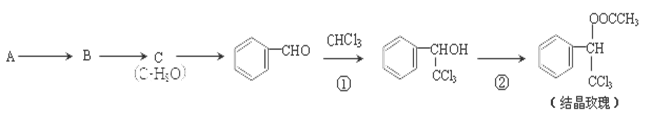
|
请回答下列问题:
(1)A→B的反应的试剂及条件是 ,B物质的类别是 。 的反应类型是 ,A的结构简式为 。
的反应类型是 ,A的结构简式为 。
酸牛奶是人们喜爱的一种营养饮料。酸牛奶中有乳酸菌可产生乳酸等有机酸,使酸碱度降低,有效地抑制肠道内病菌的繁殖。酸牛奶中的乳酸可增进食欲,促进胃液分泌,增强肠胃的消化功能,对人体具有长寿和保健作用,乳酸的结构为:
工业上它可由乙烯来合成,方法如下:
(提示:(1)CH3Cl+NaOH CH3OH+NaCl,(2)
CH3OH+NaCl,(2) 的加成类似于
的加成类似于 的加成)
的加成)
(1)乳酸所含的官能团的名称是 .
(2)写出下列转化的化学方程式:
①A的生成 .
②C的生成 .
③乳酸在一定条件合成聚乳酸 .
(3)写出符合下列要求的乳酸的所有同分异构体的结构简式
a、属于酯类b、含有-OH c、能发生银镜反应
以石油裂解产物烯烃为原料合成一些新物质的路线如下。
已知:Diels-Alder反应为共轭双烯与含有烯键或炔键的化合物相互作用生成六元环状化合物的反应,最简单的Diels-Alder反应是
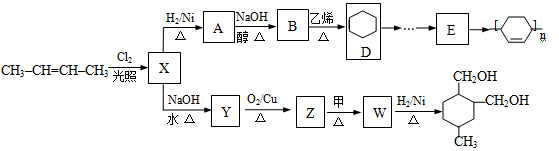
完成下列填空:
(1)写出X分子中所含官能团的名称 。
(2)写出甲物质的名称 。
(3)写出下列化学方程式:
A→B ;
E →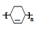 ;
;
Z→W 。
(4)属于酯类且分子中含有两个甲基的Y的同分异构体有 种。
(5)R是W的一种同分异构体,R遇FeCl3溶液显紫色,但R不能与浓溴水反应,
写出R的结构简式 。
(6)写出实验室由D制备E的合成路线。
(合成路线常用的表示方式为: )
)
从薄荷油中得到一种烃A(C10H16),叫α非兰烃,与A相关反应如下:
已知:
(1)H的分子式为____________。
(2)B所含官能团的名称为____________。
(3)含两个—COOCH3基团的C的同分异构体共有________种(不考虑手性异构),其中核磁共振氢谱呈现2个吸收峰的异构体的结构简式为______________。
(4)B→D,D→E的反应类型分别为______________、____________。
(5)G为含六元环的化合物,写出其结构简式:______________。
(6)F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂名称为___________。
(7)写出E→F的化学反应方程式:_________________________。
(8)A的结构简式为____________,A与等物质的量的Br2进行加成反应的产物共有_____种
(不考虑立体异构)。
高分子材料PET聚酯树脂和PMMA的合成路线如下:
已知:
Ⅰ. RCOOR’+ R’’18OH RCO18OR’’+R’OH(R、R’、R’’代表烃基)
RCO18OR’’+R’OH(R、R’、R’’代表烃基)
Ⅱ.  (R、R’代表烃基)
(R、R’代表烃基)
(1)①的反应类型是 。
(2)②的化学方程式为 。
(3)PMMA单体的官能团名称是 、 。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为 。
(5)G的结构简式为 。
(6)下列说法正确的是 (填字母序号)。
a.⑦为酯化反应
b.B和D互为同系物
c.D的沸点比同碳原子数的烷烃高
d.1 mol  与足量NaOH溶液反应时,最多消耗4 mol NaOH
与足量NaOH溶液反应时,最多消耗4 mol NaOH
(7)J的某种同分异构体与J具有相同官能团,且为顺式结构,其结构简式是 。
(8)写出由PET单体制备PET聚酯并生成B的化学方程式 。