【化学—选修3:物质结构与性质】金属铝、铁、铜与人类生产、生活息息相关。
(1)基态铝原子核外处在能量最高的能级上的电子共有 种不同的运动状态,工业电解熔融氧化铝时要添加助熔剂Na3[AlF6]。由氟化钠和硫酸铝可以制取Na3[AlF6],反应的化学方程式为 。
(2)聚合硫酸铁(简称PFS)的化学式为[Fe(OH)n(SO4)(3—n)/2]m,是常用的水处理剂,与PFS中铁元素价态相同的铁离子的电子排布式为 ,SO42-的空间构型是 。
(3)下列关于[Cu(NH3)4]SO4、K4[Fe(CN)6]、Na3[AlF6]的说法中正确的有_____ (填字母)。
a.三种物质中含有的化学键类型均有离子键和配位键
b.三种物质的组成元素中电负性最大与最小的两种非金属元素形成的晶体属于离子晶体
c.三种物质的组成元素中第一电离能最大的是氮元素
d.K4[Fe(CN)6]与Na3[AlF6]的中心离子具有相同的配位数
(4)某种含Cu2+的化合物可催化氧化丙烯醇(HOCH2CH=CH2)制备丙醛(CH3CH2CHO),在丙烯醇分子中共有 个σ键,其中碳原子的杂化方式是 。
(5)用晶体的X射线衍射法可以测得阿伏加德罗常数的值。对金属铜的测定得到以下结果:铜晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.0 g/cm3,则铜原子的直径约为________pm,阿伏加德罗常数的值为_______。
一定温度下,将3molA气体和1molB气体通过一密闭容器中,发生如下反应:
3A(g)+B (g) xC(g)。
xC(g)。
请填写下列空白:
(1)若容器体积固定为2L,反应1min时测得剩余1.8molA,C的浓度为0.4mol/L。
①1min内,B的平均反应速率为_________;x=__ _______;
_______;
②若反应经2min达到平衡,平衡时C的浓度_________0.8mol/L(填“大于”、“等于”或“小于”);
③平衡混合物中,C的体积分数为22%,则A的转化率是_________;
④改变起始物质加入的量,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应满足的关系式_________。
(2)若维持容器压强不变 ,达到平衡时C的体积分数_________22%,(填“大于”、“等于”或“小于”)
(16分 )镁可与其他金属构成合金。镁铝合金的强度高,机械性能好。有“国防金属”的美誉。自然界中的镁元素主要存在于海水中。海水中镁的总储量约为1.8×1015t。从海水中(主要含含Na+,Cl—,Mg2+等离子)提取镁的工艺流程图如下:
)镁可与其他金属构成合金。镁铝合金的强度高,机械性能好。有“国防金属”的美誉。自然界中的镁元素主要存在于海水中。海水中镁的总储量约为1.8×1015t。从海水中(主要含含Na+,Cl—,Mg2+等离子)提取镁的工艺流程图如下:
(1)A物质的化学式为。操作1的名称为。
(2)试写出向固体A中加入足量盐酸的离子方程式。
(3)该反应的副产物主要有等。
(4)若开始得到的固体A的质量为116g,不考虑物质的损失,则最后生成的Mg的物质的量为mol。
Ⅰ.糕点等食品包装入一个类似干燥剂的小袋――脱氧剂。其作用是吸收氧气,使食物因缺氧而不变质、发霉等,从而长期保存食品。铁脱氧剂就是利用铁易被氧化的性质来吸收氧气,最终产物是Fe2O3∙3H2O。有关反应如下:
①2Fe+O2+2H2O==2Fe(OH)2②4Fe(OH)2+O2+2H2O==4Fe(OH)3
③2Fe(OH)3==Fe2O3∙3H2O
(1)以上反应中,属于氧化还原反应的是(填编号);
(2)反应②中的还原剂是(填化学式)。
Ⅱ.黑火药是由硫黄粉、 硝酸钾和木炭按一定比例混合而成的,爆炸时的反应是:
硝酸钾和木炭按一定比例混合而成的,爆炸时的反应是:
S + 2KNO3 + 3C = K2S+ M + 3CO2↑(已配平)
(1)生成物M的化学式为;
(2)在此反应中的还原剂为。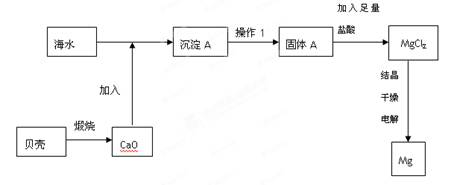
在碱性废水的处理中,通常用于烟道气处理。在充分燃烧的烟道中,大约含有14%的CO2,将烟道气通入碱性废水中进行中和处理,是比较先进而经济的办法,写出该处理方法的离子方程式。
把下列离子方程式改写成化学方程式
(1)CO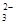 +2H+
+2H+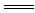 CO2↑+H2O
CO2↑+H2O
(2)Ag++Cl-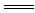 AgCl↓
AgCl↓
(3)Cu2++2OH-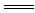 Cu(OH)2↓
Cu(OH)2↓
(4)Ba2+十SO42-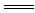 BaSO4
BaSO4 ↓
↓