下列实验装置设计正确、且能达到目的的是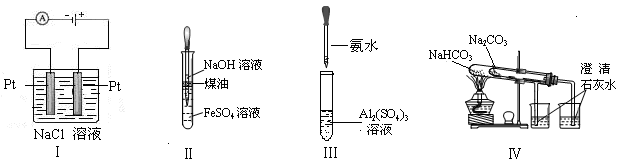
| A.实验Ⅰ:制备金属钠 | B.实验Ⅱ:制取氢氧化亚铁并观察其颜色 |
| C.实验Ⅲ:制取少量的氢氧化铝 | D.实验Ⅳ:比较两种物质的热稳定性 |
在通常状况下,下列各组气体能共存,且都能用浓H2SO4干燥的是()
| A.O2、H2S、CO2 | B.H2、NH3、Cl2 |
| C.O2、N2、SO2 | D.CO、CO2、HI |
将7. 68 g铜粉与一定质量浓硝酸反应,当铜完全作用时,收集到气体4.48 L(标况下),则所消耗硝酸的物质的量是()
| A.0.44 mol | B.0.33 mol | C.0.22 mol | D.0.11 mol |
一定条件下,某密闭容器中充入等物质的量的A、B两种气体,发生反应:
A(g) + B(g)  2C(g)。达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化如下两图所示。下列说法中正确的是()
2C(g)。达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化如下两图所示。下列说法中正确的是()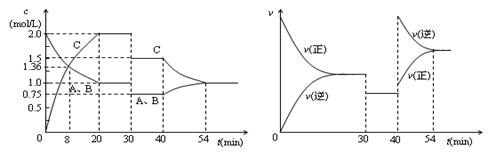
A.30min时减小容积
B.40min时加入催化剂
C.0~8min内A的平均反应速率为0.17 mol/(L·min) -1
D.正反应为放热反应
新型 NaBH4/H2O2燃料电池(DBFC)的结构如右图,(已知硼氢化钠中氢为-1价),有关该电池的说法正确的是()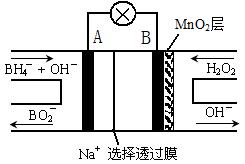
A.电极B材料中含MnO2层,MnO2可增强导电性
B.电池负极区的电极反应为:BH4 + 8OH
+ 8OH —8e
—8e = BO
= BO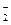 + 6H2O
+ 6H2O
C.放电过程中,Na+从正极区向负极区迁移
D.在电池反应中,每消耗1L 6 mol/LH2O2溶液,理论上流过电路中的电子为6NA个
在硫酸工业生产中,为了有利于SO2的转化, 且能充分利用热能,采用了中间有热交换器接触室(见右图)。按此密闭体系中气体的 流向,则在A处流出的气体为()
| A.SO2 | B.SO3、O2 |
| C.SO2、、SO3 | D.SO2、O2 |