已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1,向密闭容器中加入2 mol SO2和1 mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是
2SO3(g) ΔH=-196.6 kJ·mol-1,向密闭容器中加入2 mol SO2和1 mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是
注:t1~t2、t3~t4、t5之后各时间段表示达到平衡状态①、②、③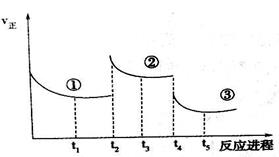
| A.t2~t3时间段,平衡向逆反应方向移动 |
| B.t4时刻改变的条件是减小压强 |
| C.平衡状态①和②,SO2转化率相同 |
| D.平衡状态①和②,平衡常数K值相同 |
下列日常生活中的现象与氧化还原反应无关的是
| A.铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
| B.用石膏点豆腐 |
| C.不良商贩用硫黄熏蒸法制作“白豆芽” |
| D.自来水厂用氯气对水进行消毒 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,22.4 L NO与11.2 L O2充分反应后得到的气体分子数为NA |
| B.3.6 g重水中含有的中子数为2NA |
| C.一定条件下,6.4 g铜与过量的硫反应,转移电子数目为0.2NA |
| D.常温下,1 L 1 mol·L-1的CH3COOH溶液中,所含溶质分子数小于NA |
H2SO4和HNO3的浓度分别为4mol/L和2mol/L的混合液,取10mL加入过量的铁粉,若HNO3的还原产物为NO,则生成气体在标况下的总体积为
| A.0.224L | B.0.672L | C.0.112L | D.0.336L |
关于Li、Na、K、Rb、Cs的叙述均正确的一组是
①金属性最强的是铯
②它们的氧化物都只有M2O和M2O2两种形式
③在自然界中均以化合态形式存在
④密度按Li—Cs顺序依次递增
⑤离子半径:Rb+>K+>Na+
| A.①②③ | B.①③④⑤ | C.②④⑤ | D.①③⑤ |
下列说法中不正确的是
| A.HF稳定性比HCl强 |
| B.Mg失电子能力比Ca弱 |
| C.NaCl与NH4Cl含有的化学键类型相同 |
| D.等物质的量的C2H6和H2O2含电子数相同 |