(10分)有机物A(C10H20O2)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。已知:
①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被Cl取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液退色。
(1)B可以发生的反应有 。
a.取代反应 b.消去反应 c.加聚反应 d.氧化反应
(2)D、F分子所含的官能团的名称依次是 、 。
(3)写出与D、E具有相同官能团的两种同分异构体的结构简式:
、 。
(4)请写出B+E →A的化学反应方程式: 。
(5)某学生检验C的官能团时,取1 mol/L CuSO4溶液和2 mol/L NaOH溶液各1 mL,在一支洁净的试管内混合后,向其中又加入0.5 mL 40%的C,加热后无砖红色沉淀出现。该同学实验失败的原因可能是 。
a.加入的C过多
b.加入的C太少
c.加入CuSO4溶液的量过多
d.加入CuSO4溶液的量不够
(12分)【化学——有机化学基础】
饱受争议的PX项目是以苯的同系物F为原料的化工项目。F中苯环上的取代基是对位关系。用质谱法测得F的相对分子质量为106,A的相对分子质量为92,A与F属于同系物。下图是以A、F为原料制得J的合成路线图。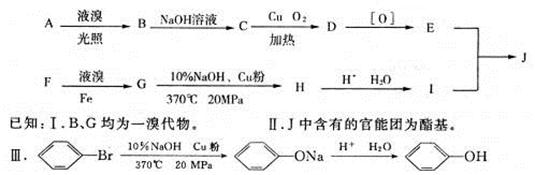
(1)写出F的结构简式:______________。
(2)C所含官能团的名称是____________。
(3)C→D的反应类型属于_____________;F→G的反应类型属于____________。
(4)写出满足以下三个条件的I的同分异构体的结构简式:______________。
i属于芳香族化合物 ii不与金属钠发生化学反应iii核磁共振氢谱有4组峰,且峰面积比为3:3:2:2。
(5)写出E和I反应最终生成J的化学方程式:____________________________________。
(1)A、B、C、D、E、F六种物质在一定条件下有如图所示的转化关系,所有反应物和生成物均已给出。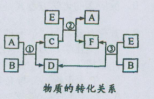
①若反应①②③均为水溶液中的置换反应,A、D、E都为卤素单质,化合物中的阳离了均为Na+,则A、D、E的氧化性由弱到强的顺序为(写化学式)。在一定条件下E和D以物质的量比为5:l在硫酸溶液中恰好完全反应,写出该反应的离子方程式:。
②若把B、C、F三种溶液汇集在一起得到1L混合溶液,并物质的转化关系给其中加入一定量的E,溶液中卤素阴离子的物质的量与通入E的体积(标准状况)的关系如下表所示(x和y均大于0)。
各离子的量与E的体积的关系
I.当通入E的体积为2.8L时,溶液中发生反应的离子方程式为。
II.x=,y=(填具体数据)。
III.当通入E的体积为11.2L时,该溶液中c(Na+)=____mol·L-1(通入E后溶液的体积变化忽略不计)。
(2)用H2O2可除去工业尾气中的Cl2,相关反应:
H2O2(1)+Cl2(g)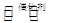 2HCl(g)+O2(g)△H>0.
2HCl(g)+O2(g)△H>0.
①为了提高H2O2的除氯效果,采取的措施最好的是(只改变一种条件),其原因是:。
(g)+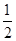 O2(g)= H2O(1), △H2 = -285.84kJ·mol-l
O2(g)= H2O(1), △H2 = -285.84kJ·mol-l
Cl2(g)+ H2(g)= 2HCl(g), △H3 = -184.6kJ·mol-l
则H2O2(1)与Cl2(g)反应生成HCl(g)和O2(g)的热化学方程式为。
[化学——有机化学基础]
香豆素是一种重要香料,以下是两种常见香豆素。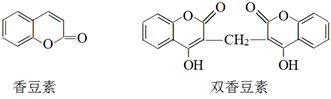
(1)关于香豆素和双香豆素,下列说法正确的是(填序号)。
| A.分子中均含有酯基 |
| B.都属于芳香族化合物 |
| C.双香豆素不能使溴水褪色 |
| D.1 mol香豆素含C=C数为4NA(NA为阿伏加德罗常数的值) |
(2)写出香豆素与足量NaOH溶液反应的化学方程式。
(3)以甲苯为原料生产香豆素流程如下: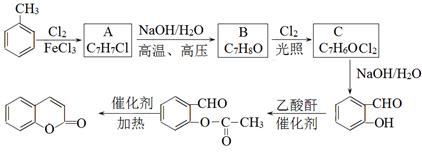
已知:(ⅰ)B可与FeCl3溶液发生显色反应;
(ⅱ)同一个碳原子上连两个羟基通常不稳定,易脱水形成羰基。
①C的结构简式是。
②B→C的反应类型是。
③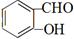 与乙酸酐(
与乙酸酐(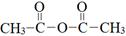 )反应,除生成
)反应,除生成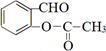 外,另一种产物是。
外,另一种产物是。
④异香豆素与香豆素互为同分异构体,具有以下特点:(a)含有苯环;(b)含有与香豆素相似的两个六元环;(c)1 mol异香豆素与足量NaOH溶液反应时消耗1 mol NaOH。写出异香豆素的结构简式。
有机物F是一种新型涂料固化剂,可由下列路线合成(部分反应条件略去)。请回答下列问题: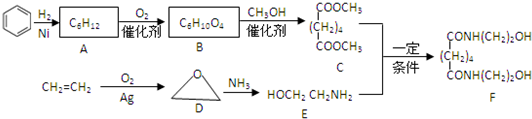
(1)B的结构简式是_______;E中含有的官能团名称是_______。
(2)由C和E合成F的化学方程式是____________________________ 。
(3)同时满足下列条件的苯的同分异构体的结构简式是______________。
①含有3个双键;②核磁共振氢谱只显示1个吸收峰;③不存在甲基
(4)乙烯在实验室可由_______(填有机物名称)通过_______(填反应类型)制备,制乙烯时还产生少量SO2、CO2及水蒸气,用以下试剂检验这四种气体,混合气体通过试剂的顺序是________。(填序号)。
①饱和Na2SO3溶液②酸性KMnO4溶液③石灰水④无水CuSO4⑤品红溶液
(5)下列说法正确的是_______(填序号)。
a.A属于饱和烃 b.D与乙醛的分子式相同
c.E不能与盐酸反应d.F可以发生酯化反应
(6)以乙烯为原料可合成乙二酸二乙酯(CH3CH2OOC-COOCH2CH3),请在方框内写出合成路线流程(无机试剂任选)。注:合成路线流程的书写格式参照如下示例:CH4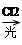 CH3Cl
CH3Cl CH3OH
CH3OH
有机物E与铜(Ⅱ)的配合物是一种可发光的发光材料,在发光器材方面有很好的应用前景。其合成E的路线如下: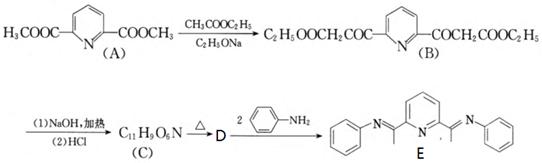
回答下列问题:
(1)B生C的反应类型有。
(2)A有多种同分异构体,其中符合以下条件的共有种。
①分子中含有吡啶环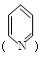 且环上只有2个取代基;
且环上只有2个取代基;
②只含有一种官能团,且核磁共振氢谱只有四种峰;
③吡啶环上的一氯取代物只有2种。
(3)C生成D的过程中有一种温室气体生成,则D的结构简式为。
(4)写出D生成E的化学方程式。
(5)结合题给信息,以 和
和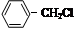 为原料合成西佛碱N-苯基苯甲亚胺(
为原料合成西佛碱N-苯基苯甲亚胺( ),请你拟出合成路线:。
),请你拟出合成路线:。