NA表示阿伏加德罗常数的值。下列判断正确的是
| A.常温常压下,17g氨气分子所含质子数为10NA |
| B.1mol Cl2参加反应,转移电子数一定为2NA. |
| C.常温常压下,22.4 L C02分子中含有2NA个σ键和2NA个π键 |
| D.1 L 0. 01 mol.L-1的Na2CO3溶液中含有0.01NA个CO32- |
用玻棒蘸取新制氯水滴在pH试纸中部,观察到的现象是: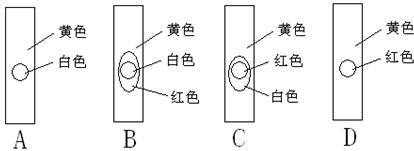
漂白粉主要成分可用下式表示:
Ca(OH)2·3CaCl(ClO)·nH2O,用过量的盐酸和漂白粉作用可生成Cl2。Cl2与漂白粉的质量比叫做漂白粉的“有效氯”。现有一种漂白粉的“有效氯”为0.355,则式中的n值约为
| A.7.5 | B.8.0 | C.9.5 | D.11.0 |
向一价金属的碘化物溶液中逐滴加入AgNO3溶液,直到沉淀完全为止。已知生成的新溶液的质量与原碘化物溶液的质量相等,则原AgNO3溶液的质量分数约为
| A.72% | B.54% | C.46% | D.28% |
标准状况下,下列关于等质量H2、D2、T2(H D T分别为氕、氘、氚)三种气体的叙述不正确的是
| A.相对分子质量之比1:2:3 | B.质子数之比 2:3:6 |
| C.中子数之比0:2:4 | D.体积之比6:3:2 |
下列实验设计和结论正确的是
| A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
B.通电时 ,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动,所以溶液是电中性的,胶体是带电的 ,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动,所以溶液是电中性的,胶体是带电的 |
| C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42— |
| D.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 |