下列各组比较中不正确的是
| A.沸点:C2H5OH>C2H6>CH4 |
| B.热稳定性:H2O>NH3>PH3 |
C.键长:—C≡C—>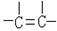 > > 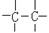 |
D.键能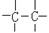 > >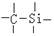 > >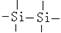 |
下列说法不正确的是 ( )
| A.均三甲苯在核磁共振氢谱中能出现两组峰,且其峰面积之比为3∶1 |
B.按系统命名法,化合物 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 |
C.结构片段为 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 |
D.肌醇 与葡萄糖 与葡萄糖 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 |
下列各组离子或分子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是 ( )
| 选项 |
离子组 |
加入试剂 |
加入试剂后发生反应的离子方程式 |
| A |
NH 、Fe2+、SO 、Fe2+、SO |
少量Ba(OH)2溶液 |
2NH +SO +SO +Ba2++2OH-===BaSO4↓+2NH3·H2O +Ba2++2OH-===BaSO4↓+2NH3·H2O |
| B |
Mg2+、HCO 、Cl- 、Cl- |
过量NaOH溶液 |
Mg2++2HCO +4OH-===2H2O+Mg(OH)2↓+2CO +4OH-===2H2O+Mg(OH)2↓+2CO |
| C |
K+、NH3·H2O、CO |
通入少量CO2 |
2OH-+CO2===CO +H2O +H2O |
| D |
Fe2+、NO 、HSO 、HSO |
NaHSO4溶液 |
HSO +H+===SO2↑+H2O +H+===SO2↑+H2O |
下列依据相关实验得出的结论正确的是 ( )
| A.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
| B.过量的铜屑与稀硝酸反应停止后,再加入1 mol/L稀硫酸,铜屑又逐渐溶解,且有无色气体产生,铜可直接与1 mol/L稀硫酸反应 |
| C.将常温下呈气态的某有机物通入溴水中,溴水褪色,该气体分子中一定含碳碳双键或碳碳三键 |
| D.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
下列对实验现象的解释与结论,正确的是 ( )
| 选项 |
实验操作 |
实验现象 |
解释与结论 |
| A |
向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热 |
无砖红色沉淀生成 |
淀粉没有水解生成葡萄糖 |
| B |
向某无色溶液中滴加硝酸酸化的Ba(NO3)2溶液 |
有白色沉淀产生 |
该溶液中一定含有SO |
| C |
向某钠盐中加入稀盐酸,将产生的气体通入澄清石灰水 |
澄清石灰水变浑浊 |
说明该盐一定是碳酸盐 |
| D |
向蔗糖中加入浓硫酸 |
变黑,放热,体积膨胀,放出刺激性气体 |
浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等 |
将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是 ( )
| A.与NaOH反应的氯气一定为0.3 mol |
| B.n(Na+)∶n(Cl-)可能为7∶3 |
| C.若反应中转移的电子为n mol,则0.15<n<0.25 |
| D.n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1 |