对某次酸雨成分的分析数据如下表,此次酸雨的c(H+)约为
| 离子 |
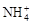 |
Na+ |
Cl― |
 |
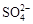 |
| 浓度(mol/L) |
2.0×10-5 |
1.9×10-5 |
6.0×10-5 |
2.3×10-5 |
2.8×10-5 |
A.1.0×10-3 B.1.0×10-4 C.2.0×10-4 D.7.2×10-5
分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是
| A.根据纯净物中的元素组成,将纯净物分为单质和化合物 |
| B.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 |
| C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D.根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类 |
下列说法不正确的是
| A.硅、二氧化硅、硅酸钠是工业上制造光导纤维的主要原料 |
| B.复合材料是将两种或两种以上性质不同的材料经特殊加工而制成的 |
| C.浓硫酸、氯化钙、五氧化二磷、碱石灰等常用作干燥剂 |
| D.氧化铝、碳酸氢钠既能与盐酸反应又能与氢氧化钠反应 |
3He可以作为核聚变材料,以下关于3He的说法正确的是
| A.比4He少一个质子 | B.比4He多一个中子 |
| C.是44He的同素异形体 | D.是4He的同位素 |
日常生活中很多问题涉及到化学知识。下列叙述错误的是
| A.用食醋清洗热水瓶中的水垢 |
| B.用米汤检验碘盐中含有碘酸钾 |
| C.用纯碱溶液洗涤餐具上的油污 |
| D.用丁达尔效应区别鸡蛋自溶液和食盐水 |
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应: SO2(g)+NO2(g)  SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如右图所示。则正确的结论是
SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如右图所示。则正确的结论是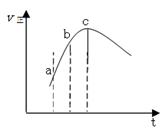
| A.逆反应速率:a点小于点c |
| B.反应物浓度:a点小于点b |
| C.反应在c点时SO2的转化率最大 |
| D.反应物的总能量低于生成物的总能量 |