相同温度和压强下,在容积为2 L的密闭容器中发生反应:2HI(g)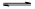 H2(g)+I2(g),达到平衡状态的标志是
H2(g)+I2(g),达到平衡状态的标志是
| A.c(H2)保持不变 |
| B.c(H2)= c(I2) |
C.2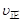 (HI)= (HI)=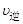 (I2) (I2) |
| D.拆开2 mol H-I共价键,同时生成1 mol H-H共价键 |
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A.质子数:c>d | B.离子的还原性:Y2->Z- |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。下列说法不正确的是( )
| A.原子半径:Y>Z>W |
| B.非金属性最强的元素为W |
| C.Y的最高价氧化物对应的水化物为强碱 |
| D.XW2分子中各原子最外层电子均达到8电子结构 |
同族元素所形成的同一类型的化合物,其结构和性质往往相似。化合物PH4I是一种白色晶体,下列对它的描述中正确的是( )
| A.它是一种共价化合物 |
| B.在加热时此化合物可以分解为PH3和HI |
| C.这种化合物不能跟碱反应 |
| D.该化合物可以由PH3和HI化合而成 |
下列各组物质中,化学键类型不同的是( )
| A.NaCl和HNO3 | B.H2O和NH3 | C. CaF2和CsCl | D.CCl4和Na2O |
、 、 、 、 是5种短周期元素,其原子序数依次增大。 是周期表中原子半径最小的元素, 原子最外层电子数是次外层电子数的3倍, 、 、 处于同一周期, 与 处于同一族, 、 原子的核外电子数之和与 、 原子的核外电子数之和相等。下列说法正确的是( )
| A. | 元素 、 、 具有相同电子层结构的离子,其半径依次增大 |
| B. | 元素 能与元素 形成化合物 |
| C. | 元素 、 分别与元素 形成的化合物的热稳定性: |
| D. | 元素 、 的最高价氧化物的水化物都是强酸 |