A、B、C、D四种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称________________;
(2)A、B形成的化合物的电子式___________________________;
(3)C的元素符号________,C的最高价氧化物的化学式_________________________;
(4)B的最高价氧化物对应水化物的浓溶液与单质Cu反应的化学方程式为____ ________
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和 部分产物未标出)
部分产物未标出)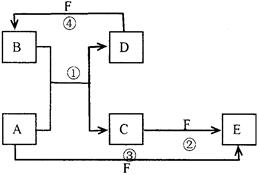
(1 ) 若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则反应④的化学方程式为:。
) 若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则反应④的化学方程式为:。
(2) 若A为金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是,
下图是煤化工产业链的一部分,试运用所学知识,解决下列问题: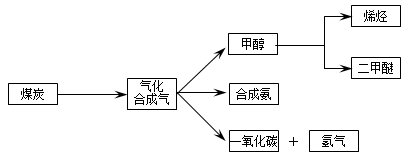
I.已知该产业链中某反应的平衡表达式为:K=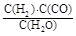 ,它所对应反应的化学方程式为。
,它所对应反应的化学方程式为。
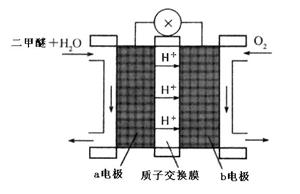
II.二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa, 温度230~280℃)进行下列反应:
温度230~280℃)进行下列反应:
①CO(g)+2H2(g) CH3OH(g)△H1=-90.7kJ·mol-1
CH3OH(g)△H1=-90.7kJ·mol-1
②2CH3OH(g) CH3OCH3(g) +H2O(g)△H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g)△H2=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g)△H3=-41.2kJ·mol-1
CO2(g)+H2(g)△H3=-41.2kJ·mol-1
(1)催化反应室中总反应的热化学方程式为。830℃时反应③的K=1.0,则在催化反应室中反应③的K1.0(填“>”、“<”或“=”)。
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2.4 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率为 ;若反应物的起始浓度分别为:c(CO)=4 mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2 mol/L,a=mol/L。
(3)为了寻找合适的反应温度,研究者进行了一系列试验,每次试验保持原料气组成、压强、反应时间等因素不变,试验结果如图.CO转化率随温度变化的规律是,其原因是.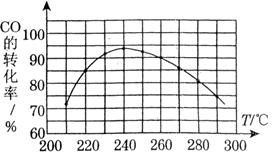
(4)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示。写出a电极上发生的电极反应式 。
。
相对分子质量不超过100的有机物A能与碳酸钠反应产生无色气体;1 mol A还可以使含溴160 g 的四氯化碳溶液恰好褪为无色;A完全燃烧只生成CO2和H2O;经分析其含氧元素的质量分数为37.21%。
(1)试写出A中含有的官能团的名称:_______________________。
(2)经核磁共振检测发现A的图谱如下:
①写出A的结构简式:。
② A具有下列性质中的(选填字母)_____________:
a.能使酸性高锰酸钾溶液褪色 b.能使溴水褪色
c.能与乙醇和浓硫酸混合液发生反应 d.能与金属钠反应
③ A在一定条件下可以发生聚合反应生成高分子化合物,写出反应的方程式:
(3)相对分子质量与A相同的某烃C有多种同分异构体,请写出其中核磁共振氢谱中峰面
积比最大的C的结构简式:。
有A、B、C、D、E、F六种元素。A是宇宙中最丰富的元素;B是周期表中电负性数值最大的元素;C的基态原子中2p轨道有三个未成对的单电子;F原子核外电子数是B与C核外电子数之和;D是主族元素,且与副族元素E同周期;E能分别形成红色(或砖红色)的E2O和黑色的EO两种氧化 物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。
物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。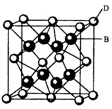
(1)E元素原子基态时的外围电子排布式为。
(2)A2F分子中F原子的杂化类型是,F的气态氧化物FO3分子的键角为。
(3)CA3极易溶于水,其原因是,试判断CA3溶于水后,形成CA3·H2O的最合理结构为(选填字母)。
(4)从晶胞结构图中可以看出,D跟B形成的离子化合物的电子式为;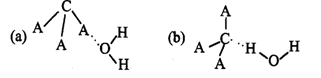
该离子化合物晶体的密度为ρ(g·cm-3)。,则晶胞的体积是(只要求列出算式)。
北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣。璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应。请回答下列问题: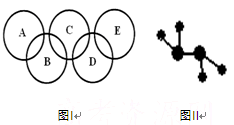
(1)火焰利用了部分金属的______反应,该反应属于______(填“物理”或“化学”)变化。
(2)右图Ⅰ所示的五圆环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素。 A是沼气的主要成分;B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型如图Ⅱ;C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3∶4,电子总数之比为3∶2。根据以上信息回答下列问题:
A是沼气的主要成分;B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型如图Ⅱ;C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3∶4,电子总数之比为3∶2。根据以上信息回答下列问题:
①B的水溶液呈弱酸性,其主要的电离方程式可表示为,D的化学式是。
② A、B、E中均含有的一种元素为(填元素名称)。
③NH3分子中的N原子有一对孤对电子,能发生反应:NH3 + HCl = NH4Cl。试写出E与足量盐酸发生反应的化学方程式。
(3)我国科研人员在实验室应用电子计算机模拟出具有高能的物质N60,它的结构与C60十分相似。已知N60分子中每个N原子均以氮氮单键结合三个氮原子,且N60结构中每个氮原子均形成8个电子的稳定结构。试推测1个N60分子的结构中含有_________个N—N键。