海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:
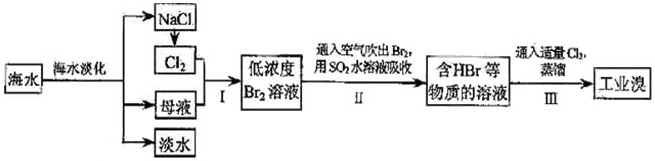
 (1)请列举海水淡化的两种方法: 、 。
(1)请列举海水淡化的两种方法: 、 。 (2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、 、 、或H2、 。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、 、 、或H2、 。 (3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 。 (4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 。 (5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,了如下装置简图:
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,了如下装置简图:
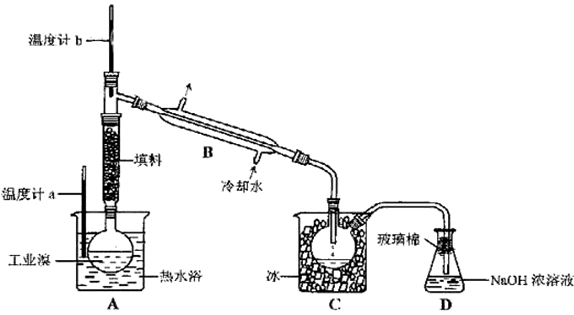
 请你参与分析讨论:
请你参与分析讨论: ①图中仪器B的名称: 。
①图中仪器B的名称: 。 ②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。 ③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: 。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: 。 ④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 。
④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 。
下列物质中含有共价键的离子化合物是
| A.BaCl2 | B.H2O | C.HCl | D.Ba(OH)2 |
重水(D2O)是重要的核工业原料,下列说法错误的是
A.氘(D)原子核外有1个电子B.1H与D互称同位素
C.H2O与D2O互称同素异形体D.1H218O与D216O的相对分子质量相同
依据元素周期表及元素周期律,下列推断正确的是
| A.H3BO3的酸性比H2CO3的强 |
| B.Mg(OH)2的碱性比Be(OH)2的强 |
| C.HCl、HBr、HI的热稳定性依次增强 |
| D.若M+和R2-的核外电子层结构相同,则原子序数:R>M |
下列说法错误的是
| A.原子及其离子的核外电子层数等于该元素所在的周期数 |
| B.元素周期表中从ⅢB到ⅡB族10个纵行的元素都是金属元素 |
| C.除氦以外的稀有气体原子的最外层电子数都是8 |
| D.同周期元素中VIIA族元素的原子半径较小 |
某元素原子的原子核外有三个电子层,最外层上的电子数是另外两个电子层电子数之差,该原子核内质子数为
| A.18 | B.16 | C.8 | D.6 |