下列各组中,每种电解质溶液电解时电解水类型的是
| A.HCl、 CuCl2、 Ba(OH)2 | B.NaOH、CuSO4、 H2SO4 |
| C.NaOH、H2SO4、 Ba(OH)2 | D.NaBr、 H2SO4、 Ba(OH)2 |
下列说法正确的是
| A.Mg的摩尔质量是24g。 |
| B.摩尔是七个基本物理量之一,符号为mol。 |
| C.同温同压下,所有气体的摩尔体积都相同。 |
| D.将40gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为1mol/L。 |
下列实验操作正确的是( )
| A.把试剂瓶中的Na2CO3溶液倒入试管中,发现取量过多,为了不浪费,又把多余的试剂倒入原试剂瓶中。 |
| B.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出。 |
| C.将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气。 |
| D.用萃取的方法分离汽油和煤油。 |
右图是常用的危险化学品标志之一,它表示的类型是( )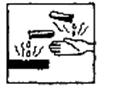
| A.腐蚀品 | B.氧化剂 |
| C.易燃品 | D.放射性物品 |
现有24mL浓度为0.05mol/L的Na2SO3溶液恰好与20mL浓度0.02mol/L的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中化合价为()
| A.+2 | B.+3 | C.+4 | D.+5 |
由二氧化碳、氢气、一氧化碳组成的混合气体在同温、同压下与氮气的密度相同。则该混合气体中二氧化碳、氢气、一氧化碳的体积比为()
| A.29∶8∶13 | B.22∶1∶14 | C.13∶8∶13 | D.26∶18∶13 |