下列化学反应中,生成物的总能量高于反应物的总能量的是
| A.Zn与盐酸反应 | B.CaO与H2O反应 |
| C.NaOH与盐酸反应 | D.C和H2O(g)反应 |
在25℃时,AgX、AgY、AgZ均难溶于水,且Ksp(AgX) = 1.8×10-10,Ksp(AgY) = 1.0×10-12,Ksp(AgZ) = 8.7×10-17。下列说法(均在25℃)错误的是
| A.三种饱和溶液中溶质的物质的量浓度的大小顺序为c(AgX)>c(AgY)>c(AgZ) |
| B.若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)减少 |
| C.若取0.188g的AgY(相对分子质量188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中Y-的物质的量浓度为1.0×10-2mol·L-1 |
| D.往C选项的溶液中加入1 mL 0.1mol·L-1的NaZ溶液,能生成AgZ沉淀 |
某溶液中含有较多的Na2SO4和少量的 Fe2(SO4)3。若用该溶液制取芒硝(Na2SO4·10H2O),可供选择的操作有:①加适量H2SO4溶液;②加金属钠;③结晶;④加过量NaOH;⑤加强热脱结晶水;⑥过滤。正确的操作步骤是
| A.②⑥③ | B.④⑥①③ | C.④⑥③⑤ | D.②⑥①③⑤ |
常温时,用某新型充电电池电解如右图所示的l00mL溶液,充电电池的总反应为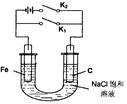
4Li+2SOCl2 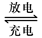 4LiCl +S+SO2,则下列叙述中不正确的是
4LiCl +S+SO2,则下列叙述中不正确的是
| A.若仅闭合K2,铁极的电极反应式:Fe - 2e=Fe2+ |
| B.放电时电池上正极的电极反应式为:2SOCl2+4e =4C1-+S+SO2 |
| C.若仅闭合K1,电子由Fe极沿导线流向C极 |
| D.若不考虑气体溶解和溶液体积变化,当电池中生成0. 025molS时,溶液中pH=14 |
有机物:C2H2 C4H4C6H6 C8H8,有关其性质叙述中不正确的是
| A.碳的质量分数相同 |
| B.固态时均为分子晶体 |
| C.一定条件下能与H2发生加成反应,就一定能使KMnO4酸性溶液褪色 |
| D.C8H8可能含有苯环结构 |
有三个容积相同的容器①②③中均发生如下反应3A(g)+ B(g) 2C(g);△H<0,①容器容积固定,外有隔热套 ②容器容积固定 ③容器有活塞可移动。下列说法正确的是
2C(g);△H<0,①容器容积固定,外有隔热套 ②容器容积固定 ③容器有活塞可移动。下列说法正确的是
A.若维持温度不变,起始时②中投人3mol A、1 mol B;③中投入3 mol A、l mol B和2mol C,则达到平衡时,两容器中B的转化率②=③
B.若起始温度相同,分别向三个容器中充入3 mol A和1mol B,则达到平衡时各容器中C物质的百分含量由大到小的顺序为③>②>①
C.若起始温度相同,分别向三个容器中充入1 mol A和1molB则达到平衡时各容器中C物质的百分含量一定相同
D.若起始温度相同,分别向三个容器中充入3a mol A和a molB则达到平衡时各容器中A物质的转化率一定相同