短周期元素A、B、C、D在周期表中所处的位置如图所示。A、B、C、D四种元素的质子数之和为36。E元素原子的半径在同周期中最大,且E的离子与C的离子具有相同的电子层结构。则下列说法正确的是
A.元素A形成的气态氢化物一定是正四面体形分子
B.五种元素形成的氢化物中,C的氢化物的沸点最高
C.A、C两种元素可形成A3C2型化合物,该化合物在空气中不能燃烧
D.B、C、D、E四种元素的离子半径由大到小的顺序为D>B>C>E
根据下列实验现象,所得结论错误的是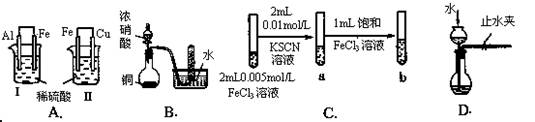
| 实验 |
实验现象 |
结论 |
| A |
Ⅰ烧杯中铁片表面有气泡,Ⅱ烧杯中铜片表面有气泡 |
活动性:Al>Fe>Cu |
| B |
试管中收集到无色气体 |
铜与浓硝酸反应产物是NO |
| C |
试管b比试管a中溶液的红色深 |
增大反应物浓度,平衡向正反应方向移动 |
| D |
长颈漏斗内液面高于烧瓶内液面且保持不变 |
装置气密性良好 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.常温常压下,44 g C3H8中含有的碳碳单键数为3 NA |
| C.标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数为3 NA |
| D.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
勤洗手和经常对环境进行消毒是预防传染病的有效途径。2012年4月,H7N9疫情爆发,可以用某种消毒液进行消毒,预防传染。已知该消毒液为无色液体,用红色石蕊试纸检验,发现试纸先变蓝后褪色,则该消毒液的主要成分可能是
| A.KMnO4 | B.H2O2 | C.NaClO | D.NH3·H2O |
下列过程属于化学变化的有
①白色的硫酸铜粉末久置于空气中变成蓝色;②同素异形体之间的互变; ③福尔马林用来浸制标本;④氯化钠溶液通电后导电;⑤蜂蚁螫咬处涂稀氨水或小苏打溶液可以减轻痛苦;⑥同分异构体之间的互变
| A.3个 | B.4个 | C.5个 | D.6个 |
在100ml硝酸和硫酸的混合液中,两种酸的物质的量浓度之和是0.6mol/l.向混合液中加入足量的铜粉,加热充分反应,所得溶液中铜离子的物质的量浓度最大值为(忽略反应前后溶液体积变化)
| A.0.30mol/l | B.0.225mol/l | C.0.45mol/l | D.0.36mol/l |