下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最快的是
| A.10℃ 20mL 3mol/L的盐酸溶液 | B.20℃ 30mL 2mol/L的盐酸溶液 |
| C.20℃ 20mL 2mol/L的盐酸溶液 | D.20℃ 10mL 4mol/L的盐酸溶液 |
白磷 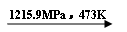 黑磷,黑磷比白磷稳定,结构与石墨相似,下列叙述正确的()
黑磷,黑磷比白磷稳定,结构与石墨相似,下列叙述正确的()
| A.黑磷与白磷互为同分异构体 | B.白磷转化为黑磷是放热反应 |
| C.白磷转化为黑磷是氧化还原反应 | D.黑磷和白磷均不能导电 |
2013年6月11日,我国“神十”载人航天飞船发射取得圆满成功。火箭发射时燃料燃烧的反应为:2 N2H4(g)+ 2NO2(g)= 3N2(g)+4H2O(l)△H=akJ/mol, 关于此反应的下列说法中正确的是
| A.a>0 |
| B.每生成1mol水,转移8mol电子 |
| C.氧化产物与还原产物的质量比为2:1 |
| D.N2H4是氧化剂 |
有机物A分子式为C2H4,可发生以下系列转化,已知B、D是生活中常见的两种有机物,下列说法不正确的是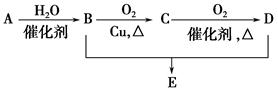
A.75%的B溶液常用以医疗消毒
B.D、E都能与NaOH溶液反应
C.B、D、E三种物质可以用饱和Na2CO3溶液鉴别
D.由B、D制备E常用浓H2SO4作脱水剂
下列鉴别方法可行的是()
| A.用氨水鉴别Al3+、Mg2+和Ag+ |
| B.用溴水鉴别苯和正己烷 |
| C.用新制Cu(OH)2悬浊液鉴别乙醇、乙醛、乙酸 |
| D.用Ca(OH)2溶液鉴别CO32-和HCO3- |
下列有关化学用语表示正确的是
A.四氯化碳分子比例模型: |
B.次氯酸的结构式为 H-Cl-O |
C.COS的电子式是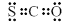 |
D.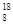 O2-离子结构示意图: O2-离子结构示意图: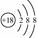 |