下列离子方程式中,书写正确的是
A.弱酸酸式盐NaHB在水溶液中水解:HB–+H2O H3O++B2– H3O++B2– |
B.电解饱和食盐水:C1-+2H2O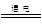 H2↑+Cl2↑+OH- H2↑+Cl2↑+OH- |
| C.氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e-=4OH- |
| D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
具有下列电子层结构的微粒,其对应的元素一定属于同一周期的是( )
| A.两原子其核外全部都是s电子 |
| B.最外层电子排布为2s22p6的原子和最外层电子排布为2s22p6的离子 |
| C.原子核外M层上的s、p能级都充满电子,而d能级上没有电子的两种原子 |
| D.两原子N层上都有1个s电子,一个原子有d电子,另一个原子无d电子 |
已知CO2、BF3、SO3都是非极性分子,NH3、H2S、H2O、SO2都是极性分子,由此可推知ABn型分子是非极性分子的经验规律是 ( )
| A.分子中所有原子在同一平面 |
| B.在ABn型分子中,A原子最外层电子不一定都成键 |
| C.在ABn分子中,A元素为最高正价. |
| D.分子中不含氢原子 |
气体分子中的极性键在红外线的照射下,易像弹簧一样做伸缩和弯曲运动,从而产生热量而造成温室效应。下列不属于温室效应气体的是( )
| A.CO2 | B.N2O | C.CH4 | D.N2 |
在以下的分子或离子中,空间结构的几何形状不是三角锥形的是()
| A.NF3 | B.CH3- | C.BF3 | D.H3O+ |
如图为元素周期表的一部分。X、Y、Z、W均为短周期元素,若W原子的最外层电子数是其次外层电子数的7/8。则下列说法中正确的是( )
| X |
Y |
|
| Z |
W |
A.Y单质可与Z的氢化物的水溶液反应,使溶液pH降低
B.最高价氧化物的水化物酸性:W>Z
C.原子半径由大到小的排列顺序是Z>Y>X
D.X的单质中有一种为白色蜡状固体