X、Y、Z、M代表四种金属,金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+离子和Z2+离子共存的溶液时,Y先析出;又知M2+离子的氧化性强于Y2+离子。则这四种金属的活动性由强到弱的顺序为
| A.M>Z>X>Y | B.X>Y>Z>M | C.X>Z>Y>M | D.X>Z>M>Y |
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:
Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是()
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是()
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
根据碘与氢气反应的热化学方程式:
(i) I2(g)+ H2(g)  2HI(g) △H="-" 9.48 kJ/mol
2HI(g) △H="-" 9.48 kJ/mol
(ii) I2(s)+ H2(g)  2HI(g) △H=+26
2HI(g) △H=+26 .48 kJ/mol
.48 kJ/mol
下列判断正确的是()
| A.254 g I2(g)中通入2gH2(g),反应放热9.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(i)的产物比反应(ii)的产物稳定 |
| D.反应(ii)的反应物总能量比反应(i)的反应物总能量低 |
下列叙述中不正确的是()
| A.某特定反应的平衡常数仅是温度的函数 |
| B.催化剂不能改变平衡常数的大小 |
| C.化学平衡发生新的移动,平衡常数必发生变化 |
| D.平衡常数发生变化,化学平衡必定发生移动,达到新的平衡 |
说法或表示法正确的是()
| A.由“C(石)→C(金);△H=" +1.9" kJ/mol ”可知金刚石比石墨稳定 |
| B.在101KPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g) = 2H2O(l);△H= -571.6kJ/mol |
| D.HCl和NaOH反应的中和热△H= -57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为△H= -(2×57.3)kJ/mol |
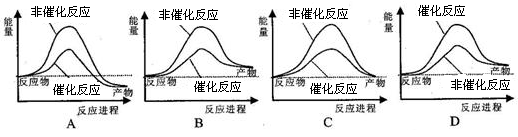
据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是()