下列各表述与示意图一致的是
| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定10 mL 0.05 mol·L-1 Ba(OH)2溶液,溶液的pH随加入酸体积的变化 |
| B.图②表示充有NO2的恒温密闭容器在t时刻增大压强时,c(NO2)随时间的变化 |
C.图③中曲线表示反应N2 (g) +3 H2(g) 2NH3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化 2NH3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化 |
D.图④中a、b曲线分别表示反应2SO2(g) + O2(g) 2SO3(g) ΔH<0使用(a)和未使用(b)催化剂时,反应过程中的能量变化 2SO3(g) ΔH<0使用(a)和未使用(b)催化剂时,反应过程中的能量变化 |
下列各组中的离子,能在溶液中大量共存的是( )
A.Al3+、NO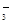 、OH-、Cl- 、OH-、Cl- |
B.H+、Ba2+、Ag+、Cl- |
C.Fe2+、Fe3+、Na+、NO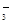 |
D.Ca2+、H+、Cl-、CO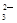 |
下列物质中,不属于电解质的是( )
| A.蔗糖 | B.H2SO4 | C.NaOH | D.NH3·H2O |
含0.5mol Na2SO4的溶液中,Na+ 约为()个
| A.0.5 | B.1 | C.3.01×1023 | D.6.02×1023 |
下列有关实验室制取气体的反应中,其原理不属于氧化还原反应的是()
| A.实验室中用稀硫酸与锌粒反应制取H2 |
| B.实验室中用高锰酸钾加热分解制取O2 |
| C.实验室中用H2O2与MnO2作用产生O2 |
| D.实验室中用稀盐酸与石灰石反应制取CO2 |
雕花玻璃总让人赏心悦目。下列物质中能对玻璃进行刻蚀而成花的是( )
| A.硅酸 | B.烧碱 | C.氢氟酸 | D.明矾 |