已知反应A2(g)+B2(g)=2AB(g),断开1molA2中的化学键消耗的能量为Q1 kJ,断开1molB2中的化学键消耗的能量为Q2 kJ,生成1molAB中的化学键释放的能量为Q3kJ(Q1、Q2、Q3均大于零),则下列说法正确的是
| A.若A2和B2的总能量之和大于生成的2AB的总能量,则反应放热 |
| B.若A2和B2的总能量之和小于生成的2AB的总能量,则反应放热 |
| C.若该反应为放热反应,则Q1+Q2 < Q3 |
| D.若该反应为吸热反应,则Q1+Q2 < Q3 |
锂和钾两种元素相比较,正确的是
| A.锂的还原性比钾的弱 | B.锂原子的半径比钾的大 |
| C.锂的金属性比钾的强 | D.锂单质的熔点比钾的低 |
X、Y、Z都是第三周期元素,核电荷数依次增大,X的氧化物对应水化物是强碱,Z的原子半径在该周期中最小。据此判断下列说法正确
| A.X是第IA 元素,Z是第ⅦA | B.元素X、Z形成的化合物是共价化合物 |
| C.Y一定是金属元素 | D.Z的最高价氧化物对应的水化物是弱酸 |
下列各对物质中,互为同分异构体的是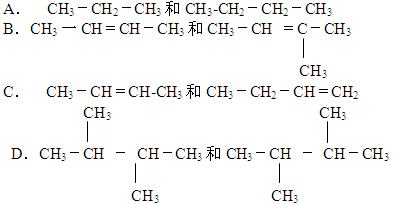
下列化学方程式中,不正确的是
| A.Zn+2HCl===ZnCl2+H2↑ | B.Al2O3+2NaOH===2NaAlO2+H2O |
| C.2Fe+3CuSO4===Fe2(SO4)3+3Cu | D.2Al+Fe2O3 2Fe+Al2O3 2Fe+Al2O3 |
下列关于卤族元素的比较中,错误的是
A气态氢化物稳定性:HF>HCl>HBr>HI B单质氧化性:F2>Cl2>Br2>I2
C.离子的还原性:F->Cl->Br->I-D.元素的非金属性:F>Cl>Br>I